.jpg)
В современной медицинской литературе модно ХХІ век называть веком различных эпидемий. Для фибрилляции предсердий (ФП) и ожирения не сделали исключения, однако в данном случае это не просто дань моде. В Украине насчитывается более 1,5 млн больных ФП. Хотя от этой аритмии не умирают, она является предиктором развития сердечной недостаточности (СН) и такого смертельного осложнения, как кардиоэмболический инсульт.
Согласно Европейским рекомендациям по ведению больных ФП, особое внимание следует уделять основному заболеванию, на фоне которого возникла аритмия (класс рекомендации I). В то же время у пациентов с ожирением снижение массы тела совместно с менеджментом других факторов риска (ФР) ассоциируется со снижением количества эпизодов ФП и уменьшением симптомов (класс рекомендаций IIA).
Без курации основного заболевания невозможно добиться адекватного влияния на пароксизмы ФП, какой бы «волшебный» антиаритмик больной не принимал. Безусловно, мы обращаем внимание на артериальную гипертензию (АГ), ишемическую болезнь сердца (ИБС), перенесенный инфаркт миокарда, СН, сопутствующий сахарный диабет (СД) и их сочетание как причину развития ФП, но так ли мы внимательны к ожирению? И есть ли какая-то взаимосвязь между ожирением и ФП? Ведь ожирение также называют эпидемией ХХІ века.
Согласно последней классификации Всемирной организации здравоохранения (ВОЗ, 2004), индекс массы тела (ИМТ) 18,5-24,9 кг/м2 считается нормальным, а ИМТ ≥30 кг/м2 позволяет говорить о «болезненном» (морбидном) ожирении. По данным ВОЗ, распространенность ожирения в экономически развитых странах не превышала 10%, в 2008 г. свыше 1,6 млрд взрослого населения планеты имели избыточный вес, в том числе более 500 млн – ожирение. В соответствии с экспертными оценками ВОЗ, к 2030 г. на планете будет проживать 2,2 млрд людей с избыточным весом и 1,1 млрд – с ожирением. В связи с этим не так давно появился термин globesity, обозначающий массовость случаев ожирения по всему миру. Так, количество лиц с ожирением в Украине с 2001 по 2012 г. увеличилось на 30,6%, и этот показатель растет каждый год.
В настоящее время результаты значительного числа эпидемиологических исследований свидетельствуют о взаимосвязи ожирения и развития сердечно-сосудистых заболеваний (АГ, ИБС, СН), СД 2 типа, онкологических заболеваний, бронхиальной астмы, болезней опорно-двигательного аппарата, поликистоза яичников у женщин, синдрома Пиквика, обструктивного апноэ во сне, депрессии, булимии. Имеются данные о более высокой частоте среди лиц с ожирением гиперхолестеринемии, нарушений реологии крови, тромбоэмболических осложнений, гипертрофии миокарда левого желудочка. В 2013 г. опубликован метаанализ 97 проспективных исследований, выполненных с 1948 по 2005 г., в котором показано, что риск развития ИБС значительно выше при избыточном весе (ИМТ 25-29,9 кг/м2) и ожирении (ИМТ ≥30 кг/м2) (относительный риск, ОР 44%); риск развития острых нарушений мозгового кровообращения на 98% выше для пациентов с избыточным ИМТ и на 69% – при ожирении (с учетом таких ФР, как повышенные уровни артериального давления, холестерина и глюкозы). По данным ВОЗ, ожирением обусловлены 44% случаев развития СД, 23% – ИБС и 7-41% – определенных видов рака. В ряде исследований подчеркивается, что ожирение увеличивает расходы на медицинскую помощь и ухудшает качество жизни больных [25-27]. Ожирение вызывает целый ряд неблагоприятных последствий для здоровья, обусловливает социальные, психологические и экономические проблемы, затрагивающие как отдельного человека, так и общество в целом [28].
В 1999 г. E. Calle и соавт. опубликовали результаты когортного исследования, в котором участвовали более 1 млн жителей США [29]. Во всех подгруппах (курящие, некурящие, мужчины, женщины, наличие или отсутствие хронических заболеваний) показатели смертности были минимальны при ИМТ 22-26 кг/м2 с небольшой вариацией в подгруппах. В дальнейшем было показано, что абдоминальное ожирение (окружность талии >88 см у женщин и >102 см у мужчин), отягощенное курением, повышает риск сердечно-сосудистых событий в 5,5 раза. В 2005 г. С. А. Шальнова и соавт. отметили, что ожирение в 2,5 раза увеличивает смертность от инфаркта миокарда у мужчин. Влияние на остальные показатели смертности от сердечно-сосудистых заболеваний у мужчин и женщин статистически незначимо [31]. В 2006 г. опубликованы результаты крупного проспективного исследования, в котором риски сердечно-сосудистой смерти у некурящих старше 75 лет рассматривались в зависимости от ИМТ и объема талии. G. M. Price и соавт. пришли к выводу, что ИМТ без учета объема талии не может быть критерием ФР сердечно-сосудистой смертности у пожилых пациентов. В 2013 г. T. Coutinho и соавт. опубликовали результаты еще одного крупного исследования (15 547 пациентов с ИБС). Было показано, что наиболее высокий риск смерти имели пациенты с нормальным ИМТ и абдоминальным ожирением (индекс объем талии / объем бедер, ИТБ 0,98): он превышал таковой у пациентов с нормальным ИМТ и ИТБ 0,89 (ОР 1,10; 95% доверительный интервал, ДИ 1,05-1,17), с избыточным весом (ИМТ – 26 кг/м2) и ИТБ 0,89 (ОР 1,20; 95% ДИ 1,09-1,31), с ожирением и ИТБ 0,89 (ОР 1,61; 95% ДИ 1,39-1,86) и даже у пациентов с ожирением и ИТБ 0,98 (ОР 1,27; 95% ДИ 1,18-1,39) [33].
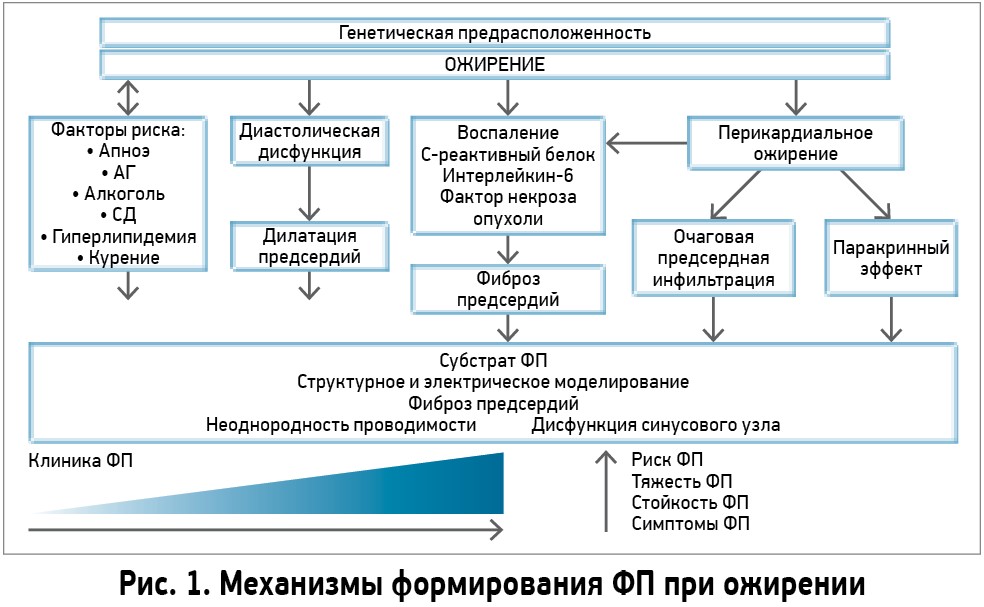
Представления о жировой ткани и ее функции в организме человека претерпели значительные изменения. Данные последних исследований преподносят ее не только как энергетическое депо, но и как эндокринный и паракринный орган, способный влиять на другие органы и системы. Эти свойства жировой ткани отличаются в зависимости от морфологии самих адипоцитов и их локализации. В отличие от подкожного жира, который составляет обычно 75% от всей жировой ткани организма и является основным хранилищем липидов, висцеральный жир (мезентериальные адипоциты) гораздо более активен как эндокринный орган. Как адипоциты, так и макрофаги жировой ткани секретируют большое количество факторов с разнообразными эффектами: влияние на метаболизм глюкозы (адипонектин, резистин и др.), липидов (белок, переносящий эфиры холестерина), на воспаление (фактор некроза опухоли, интерлейкин‑6), коагуляцию (ингибитор активатора плазминогена‑1), регуляцию давления крови (ангиотензин II, ангиотензиноген), пищевое поведение (лептин), а также на метаболизм и функциональную активность различных органов и тканей, в том числе мышц, печени, мозга и сосудов. При висцеральном ожирении развиваются процессы ремоделирования жировой ткани: гипертрофия адипоцитов, активация медленно прогрессирующего воспаления, нарушение ангиогенеза, избыточное накопление коллагена и фиброз делают ее дисфункциональной, что характеризуется сдвигом равновесия в сторону продукции большего количества провоспалительных и атерогенных цитокинов. Именно поэтому ряд ученых считают патологическое ожирение хроническим системным воспалительным процессом (рис. 1).
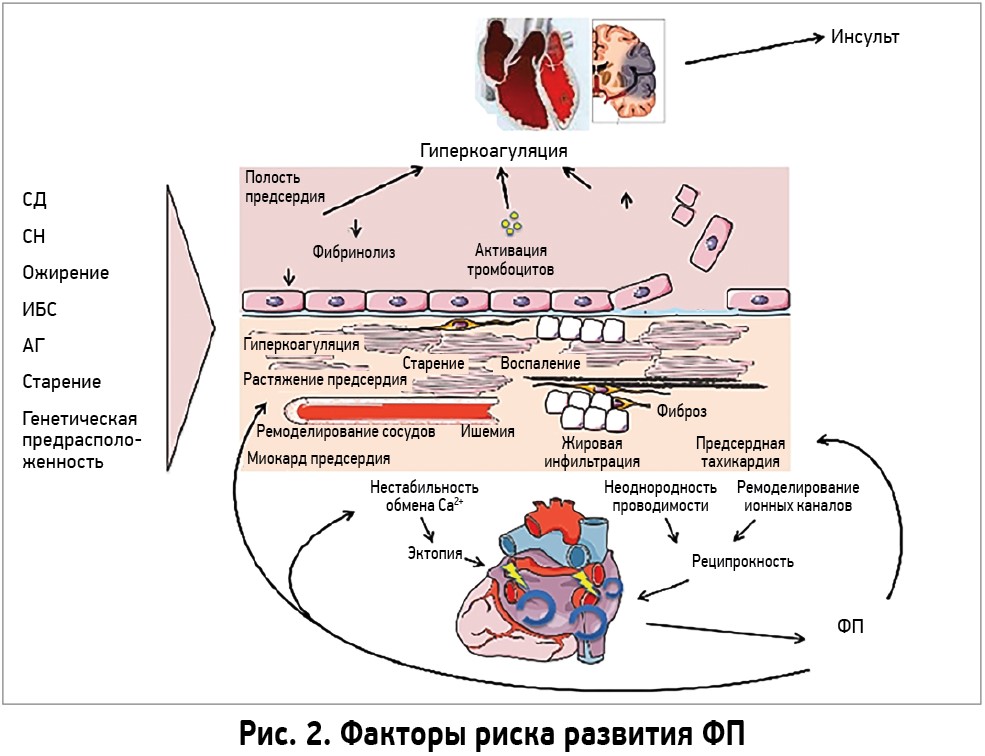
Взаимосвязь ФП и ожирения существует. Так, в Европейских рекомендациях по ведению больных ФП ожирение представлено как ФР развития данной аритмии (рис. 2).
В опубликованном в журнале JAHA исследовании отмечается, что мужчины и женщины, страдающие избыточным весом или ожирением, подвержены повышенному риску развития ФП. Используя данные 24 799 взрослых норвежцев, исследователи проанализировали связь между изменением ИМТ и риском развития ФП. Наблюдение продолжалось в течение 16 лет. За это время ФП развилась у 811 (6,2%) мужчин и 918 (7,9%) женщин. Результаты показали, что даже при наличии незначительного избыточного веса увеличение ИМТ было связано с повышенным риском ФП. Например, по сравнению с ИМТ 23 кг/м2, попадающим в диапазон здорового веса, у мужчин с ИМТ 25 кг/м2 вероятность развития ФП увеличивалась на 14%. Вместе с тем ИМТ 18 кг/м2, свидетельствующий о недостаточном весе, был связан со снижением риска ФП на 25% по сравнению с ИМТ 23 кг/м2. Среди женщин была выявлена схожая картина. У мужчин и женщин уменьшение ИМТ с течением времени ассоциировалось со снижением риска ФП, а увеличение ИМТ – с повышением риска ФП.
Весьма интересной и масштабной представляется работа N. Echahidi и соавт. (2007) [6], в которой оценивались ФР развития ФП после операции аортокоронарного шунтирования. Авторы указывают, что ФП – весьма распространенное осложнение после операций на сердце, существенно влияющее на прогноз. В предыдущих исследованиях уже было показано, что ФР после операций является ожирение. Был проведен ретроспективный анализ взаимосвязи между ожирением и метаболическим синдромом (МС), а также пароксизмальной ФП у 5085 пациентов после аортокоронарного шунтирования. У 1468 (29%) пациентов было ожирение (ИМТ ≥30 кг/м2), у 2320 (46%) – МС в соответствии с критериями ATP-III. Пароксизмальная ФП возникла у 1374 (27%) пациентов. При ожирении пароксизмы ФП возникали достоверно чаще только у больных старше 50 лет. Однако МС в отсутствие ожирения также оказался независимым значимым ФР развития ФП (12 против 6%), вне зависимости от возраста.
Важным условием для возникновения ФП является наличие структурных изменений сердца, таких как гипертрофия и ишемия миокарда, дилатация желудочков, фиброзные изменения стенки сердца. При наличии этих изменений и влиянии внешних факторов создаются условия для формирования электрической нестабильности предсердий, что приводит к формированию петель re-entry и срыву ритма. По данным исследований, ожирение является важным ФР возникновения и поддержки ФП [1, 4, 5].
ФП опосредована дилатацией левого предсердия, так как наблюдается постепенное увеличение его размера соответственно увеличению ИМТ от нормального до избыточного. Анализ публикаций о взаимосвязи ожирения и структурных изменений миокарда дает возможность выделить следующие механизмы: аккумуляцию триглицеридов сыворотки крови в миокарде [13], которая приводит к миокардиальному стеатозу, повышенной массе миокарда левого желудочка, дилатации полостей сердца с формированием систолической и диастолической дисфункции левого желудочка [9, 15].
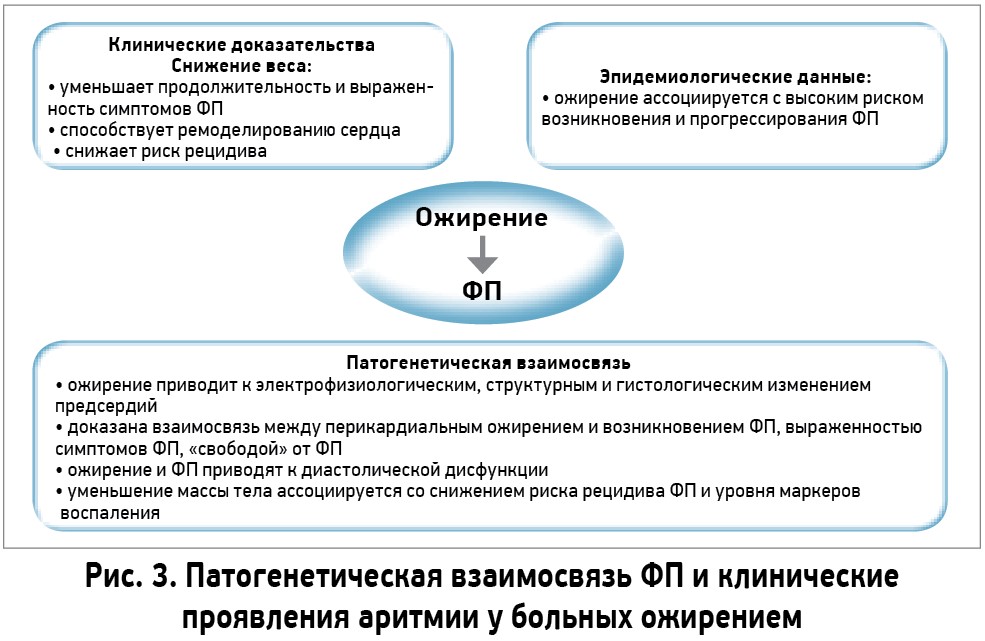
Таким образом, наличие ожирения у больных с сердечно-сосудистыми заболеваниями обусловливает дисфункцию миокарда и появление проаритмогенного эффекта. Схематически механизмы ФП при ожирении и клинические эффекты представлены на рисунке 3.
При обследовании больных ФП следует анализировать не только взаимосвязь ожирения и дебюта аритмии, но и влияние ожирения на частоту рецидива ФП, то есть кратность пароксизмов, их длительность и клиническую окраску. Согласно данным исследования LEGAСY, коррекция веса у больных ФП без использования антиаритмической терапии (ААТ), подвергшихся процедуре абляции и без таковой, позволила уменьшить кратность пароксизмов ФП и тяжесть симптомов. Длительность наблюдения составила 4 года (рис. 4). У пациентов, снизивших свой вес более чем на 10% от исходного, реже возникали рецидивы ФП, чем у пациентов с меньшим процентом коррекции веса.
В 2013 г. вышли совместные рекомендации Американской ассоциации сердца (AHA), Американского колледжа кардиологии (ACC) и Общества по изучению проблем ожирения (TOS), посвященные ведению больных с ожирением. Первым пунктом в них значится модификация образа жизни. Целью консервативного лечения ожирения является снижение массы тела на 5-10% за 3-6 мес терапии и удержание результата в течение года, что позволяет уменьшить риски для здоровья, улучшить течение заболеваний, ассоциированных с ожирением. Изменение образа жизни посредством коррекции питания и увеличения объема физических нагрузок является основой в лечении ожирения и рекомендуется как первый и постоянный этап терапии. Для большинства пациентов, страдающих морбидным ожирением, изменение питания на длительный период времени представляет невыполнимую задачу. Снижение калорийности питания на 500-1000 ккал в сутки от расчетного приводит к уменьшению массы тела на 0,5-1,0 кг в неделю. Такие темпы снижения веса сохраняются в течение 3-6 мес. В дальнейшем умеренное снижение массы тела приводит к уменьшению энергозатрат на 16 ккал/кг в сутки у мужчин и на 12 ккал/кг в сутки у женщин за счет уменьшения тощей массы, в результате чего потеря веса приостанавливается. Физическая активность рекомендуется как неотъемлемая часть лечения ожирения и поддержания достигнутой массы тела (уровень доказательности 1). Для ряда пациентов расширение режима физической активности невозможно в связи с наличием патологии опорно-двигательного аппарата и/или сердечной и дыхательной недостаточности.
Назначение фармакологических препаратов для лечения ожирения рекомендуется при ИМТ ≥30 кг/м2 или при наличии ассоциированных с ожирением заболеваний у пациентов с ИМТ 27-29,9 кг/м2. Однако с медикаментозной терапией в Украине дело обстоит не просто. Препараты, ингибирующие обратный захват серотонина в центральной нервной системе (фенфлурамин, дексфенфлурамин, фенилпропаноламин), а также норадренергические анорексигенные препараты с механизмом подавления аппетита (фентермин; диэтилпропион, мазиндол) сняты с регистрации, а селективный ингибитор каннабиноид‑1 рецептора эндоканнабиноидной системы римонабант и ингибитор обратного захвата серотонина и норадреналина сибутрамин запрещены в 2009 и 2010 г. соответственно. Зарегистрирован и разрешен к использованию препарат, уменьшающий всасывание нутриентов (орлистат).
Способствовать снижению массы тела может употребление диетических добавок к рациону питания. На рынке Украины и некоторых странах Евросоюза присутствует продукт Ингуар. Его активным компонентом является смола гуаровая – пищевая клетчатка из эндосперма семян Cyamopsis tetragonolobus, полисахарид, образующий с водой вязкий гель. Механизм действия смолы гуаровой хорошо изучен и заключается в снижении всасывания углеводов и жиров в тонком кишечнике. Поскольку смола гуаровая не абсорбируется, не существует противопоказаний для ее употребления в период беременности и кормления грудью.
Прием Ингуара позволяет увеличить потребление клетчатки, которая является пищей для полезной микробиоты кишечника и которой катастрофически мало в рационе современного человека. Компоненты смолы гуаровой частично разлагаются под действием кишечных бактерий на короткие цепочки жирных кислот и увеличивают количество каловых масс примерно на 20%. Таким образом, при использовании продукта Ингуар возможно сбалансировать рацион питания, уменьшить чувство голода, тем самым снизить количество потребляемой пищи и нормализировать пищеварение. Применение Ингуара в течение 2-3 мес позволяет не только добиться снижения уровня холестерина и глюкозы в крови, но и сформировать правильные пищевые привычки, которые приведут к физиологической потере массы тела.
Представляю собственный опыт использования продукта Ингуар. В начале 2019 г. ко мне на прием пришел мужчина 49 лет с жалобами на частые пароксизмы ФП. Прежде всего бросилось в глаза ожирение
Подводя итоги, хотелось бы подчеркнуть: при ведении пациента с ФП необходимо учитывать коморбидности. Добиться успеха в лечении аритмии возможно, только влияя на все ФР развития пароксизмов и сопутствующую патологию.