Лайм-бореліоз — зоонозна інфекція з трансмісивним механізмом передачі, яку спричиняють мікроорганізми Borrelia burgdorferi (рідше — B. mayonii). Природним резервуаром борелій є гризуни, птахи, олені та велика рогата худоба. Переносником борелій між тваринами та людиною є іксодові кліщі (Ixodes scapularis та I. pacifcus): людина заражається при укусі кліща, інфікованого бореліями. Можливість передачі Лайм-бореліозу від людини до людини на сьогодні не доведена.
Лайм-бореліоз є найпоширенішим трансмісивним інфекційним захворюванням, яке характеризується широким поліморфізмом клінічних проявів. Найбільша кількість захворювань реєструється у весняно-осінній період (травень–жовтень), що пов’язано зі збільшенням проведення часу на відкритому повітрі та сезонною активністю кліщів (найбільш активні у квітні–червні та серпні–жовтні).
У публікації висвітлено клінічну картину Лайм-бореліозу, сучасний алгоритм діагностики та схеми лікування інфекції, а також показання до проведення постконтактної профілактики Лайм-бореліозу при укусі кліща.
Рання локалізована стадія Лайм-бореліозу: клінічна картина та особливості діагностики
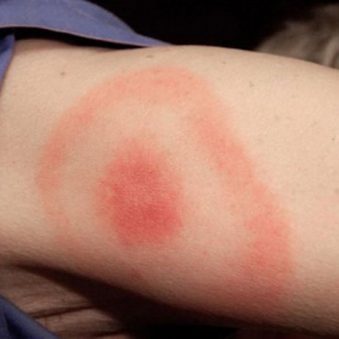
Рання локалізована стадія Лайм-бореліозу виникає через 1–30 днів (у середньому через 7 днів) після укусу інфікованого кліща. Патогномонічним симптомом цієї стадії захворювання є поява ізольованої мігруючої еритеми на місці інокуляції збудника (найчастіше у пахвовій, пахвинній або підколінній ділянках). Мігруюча еритема ідентифікується у 50–90% пацієнтів із Лайм-бореліозом.
Зазвичай на місці укусу кліща спочатку з’являється папула або червона пляма з ущільненням, яка чітко відмежовується від здорової шкіри. Згодом на її місці може утворюватися везикула чи пустула (первинний афект). Поступово ділянка гіперемії центробіжно розширюється («мігрує»), а центр бліднішає, що створює вигляд кільцеподібної мігруючої еритеми. У більшості випадків діаметр еритеми >5 см та може досягати 50 см. Мігруюча еритема може бути однорідною еритематозною, а не кільцеподібною. У деяких випадках відзначається регіонарний лімфаденіт. Загальний стан хворих під час ранньої локалізованої стадії Лайм-бореліозу зазвичай задовільний.
Мігруюча еритема зберігається декілька днів–тижнів, після чого зникає, залишаючи після себе пігментацію чи лущення. У 1/3 осіб захворювання самостійно завершується на цій стадії, а у 2/3 — переходить на наступну — ранню дисеміновану стадію.
Мігруюча кільцеподібна еритема — патогномонічна ознака Лайм-бореліозу. Наявність мігруючої еритеми при встановленому контакті з кліщем в ендемічній ділянці є достатнім аргументом для клінічного встановлення діагнозу та початку специфічної антибіотикотерапії без подальших досліджень. Серологічні дослідження на ранній локалізованій стадії Лайм-бореліозу часто негативні: перші антитіла зазвичай з’являються лише через 3–6 тиж від моменту укусу кліща.
Рання дисемінована стадія Лайм-бореліозу: характерна полісистемність уражень
Через декілька днів після завершення ранньої локалізованої стадії захворювання переходить у наступну фазу — ранню дисеміновану, для якої характерне гематогенне розповсюдження збудника та генералізація інфекційного процесу. На фоні генералізації процесу можлива поява нових плям (зазвичай менших розмірів, ніж первинна мігруюча еритема) на різних ділянках тіла — множинних мігруючих еритем. Нерідко виникає короткочасний розеольозний, папульозний або уртикарний висип. Рідкісним шкірним проявом Лайм-бореліозу є так звана бореліозна лімфоцитома — одиничне синювато-червоне утворення, яке може локалізуватися на мочці вуха, поблизу соска чи в ділянці мошонки.
Генералізація інфекційного процесу супроводжується підвищенням температури тіла (не завжди), появою головного болю, міалгією. Характерна полісистемність уражень з розвитком неврологічних (параліч лицевого та інших пар черепних нервів, менінгорадикулопатія (синдром Баннварта), асептичний менінгіт), серцево-судинних (атріовентрикулярні блокади, міокардит, перикардит) проявів, появою мігруючої артралгії (ураження переважно великих суглобів без об’єктивних ознак артриту), ураженням очей (ірит, іридоцикліт, панофтальміт тощо). У частини хворих можлива поява генералізованої лімфаденопатії.
Таким чином, рання дисемінована стадія характеризується полісистемністю уражень із тенденцією до самозавершення та виникає внаслідок гематогенного розповсюдження збудника. Тривалість ранньої дисемінованої стадії зазвичай становить 3–6 тиж.
Пізня стадія Лайм-бореліозу: характерне ураження переважно однієї системи
Пізня стадія Лайм-бореліозу розвивається через місяці–роки після інфікування та переважно характеризується ураженням однієї системи (Лайм-артрит, хронічний атрофічний акродерматит або нейробореліоз). В основі клінічних проявів, характерних для пізньої стадії Лайм-бореліозу, — аутоімунні реакції.
Лайм-артрит характеризується ураженням переважно великих суглобів (зазвичай колінних, рідше — кульшових, плечових та ін.) з чергуванням періодів загострень (кілька тижнів–місяців) та ремісій. Ураження дрібних суглобів не характерне.
Дерматологічні прояви на пізній стадії Лайм-бореліозу характеризуються розвитком хронічного атрофічного акродерматиту — повільно прогресуючого ураження шкіри з появою блакитно-червоних плям переважно на розгинальних поверхнях дистальних відділів кінцівок та подальшої атрофії шкіри.
Ураження нервової системи, характерні для пізньої стадії Лайм-бореліозу (пізній нейробореліоз), включають енцефалопатію, периферичну нейропатію (помірну дифузну полінейропатію за типом рукавичок та шкарпеток) та розсіяний енцефаломієліт.
Серологічна діагностика Лайм-бореліозу: етапи та інтерпретація
Діагноз Лайм-бореліозу встановлюється на основі характерної клінічної картини та двоетапного серологічного підтвердження. Двоетапність серологічної верифікації має ключове значення у діагностиці Лайм-бореліозу та включає:
- перший етап (імунофлуоресцентний аналіз — ІФА) — визначення титрів імуноглобулінів (Ig) класу M та G методом ІФА.
− Якщо результат ІФА негативний та:
- дослідження проводилося протягом перших 30 днів від початку симптомів — повторити ІФА через 4–6 тиж після першого дослідження ІФА;
- дослідження проводилося через ≥30 днів з моменту появи симптомів — подальші обстеження не проводяться, необхідно підозрювати альтернативний діагноз;
− Якщо результат ІФА сумнівний або позитивний → підтвердження діагнозу методом вестерн-блот;
- другий етап (вестерн-блот) — проводиться лише у разі підтвердженого чи сумнівного результату ІФА. Недоцільно проводити вестерн-блот без попереднього етапу діагностики методом ІФА. При цьому:
− якщо симптоми захворювання наявні <30 днів — методом вестерн-блот проводиться визначення IgG та IgM;
− якщо симптоми захворювання наявні >30 днів — методом вестерн-блот проводиться визначення лише IgG.
Вестерн-блот — високочутлива та високоспецифічна діагностична методика, спрямована на визначення IgM та IgG до специфічних антигенів борелій. Тлумачення результату вестерн-блоту потребує від лікаря знань щодо правил інтерпретації результату. Алгоритм інтерпретації результатів вестерн-блоту представлений у табл. 1.
Таблиця 1. Алгоритм інтерпретації результатів дослідження при виявленні антитіл методом вестерн-блоту
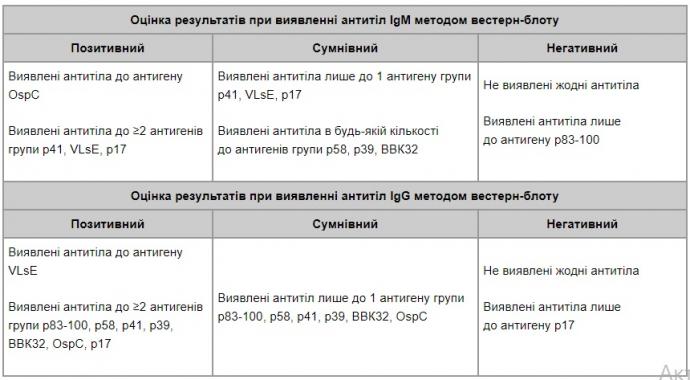
Якщо при проведенні дослідження виявляються позитивні IgM та негативні IgG, необхідно провести повторний вестерн-блот через 2 тиж. Якщо повторне дослідження продовжує відображати аналогічний результат (IgM+, IgG–), його слід розцінювати як хибнопозитивний (може бути результатом перехресної реакції антитіл при сифілісі, аутоімунних захворюваннях).
Інші методи діагностики Лайм-бореліозу: ПЛР та визначення синтезу інтратекальних антитіл
Для діагностики Лайм-артриту може застосовуватися молекулярно-генетичне та серологічне дослідження синовіальної рідини, результати яких практично завжди позитивні. Якщо антибіотикотерапія не зумовлює полегшення проявів Лайм-артриту, слід запідозрити антибіотик-рефрактерний Лайм-артрит. У цьому разі результати ПЛР синовіальної рідини зазвичай негативні.
Золотим стандартом діагностики нейробореліозу є визначення синтезу інтратекальних антитіл: співвідношення рівнів IgG у лікворі/сироватці крові >1,0 свідчить проаактивне інтратекальне утворення антитіл та підтверджує діагноз нейробореліозу. Зміни в лікворі при цьому зазвичай характеризуються помірним лімфоцитарним плеоцитозом (<1000 кл/мкл) та підвищенням рівня білка. ПЛР-дослідження ліквору має низьку чутливість, у той час як серологічні дослідження практично завжди відображають позитивний результат.
Пряма ідентифікація борелій у кліщах після їх вилучення не рекомендована
Згідно з настановами Європейського товариства клінічної мікробіології та інфекційних хвороб (European Society of Clinical Microbiology and Infectious Diseases — ESCMID), дослідження кліщів на наявність антигенів або ДНК борелій не рекомендоване, оскільки:
- В Європі близько 20–25% кліщів є інфікованими бореліями, тоді як ризик розвитку інфекції з клінічними симптомами після укусу кліща становить 1–5% (тобто 1 випадок на 20–100 укусів кліщів).
- Позитивний результат дослідження вказує на те, що кліщ містив борелії, проте не дозволяє спрогнозувати ризик інфікування людини.
- Трансмісія борелій протягом перших 24 год прикріплення кліща є малоймовірною.
- Антибіотикотерапія показана за наявності клінічних симптомів захворювання та не повинна базуватися на результаті дослідження кліщів.
- У жодному дослідженні, результати якого були опубліковані, не оцінювали якості тестів, які застосовують для ідентифікації борелій у кліщах, та не намагалися їх стандартизувати.
- Описані випадки Лайм-бореліозу при негативних результатах дослідження вилучених кліщів на наявність борелій.
- Негативний результат тесту може створити для людини хибне відчуття безпеки, спричинити нехтування перевіркою шкіри на наявність ознак запалення та затримувати діагностику.
- Використання високовартісних тестів для визначення борелій у кліщах може призвести до надмірного лікування неінфікованих пацієнтів.
Таким чином, організація ESCMID не рекомендує проводити дослідження кліщів на наявність борелій після їх вилучення з метою прогнозування ризику розвитку Лайм-бореліозу та прийняття рішення щодо подальшого менеджменту.
Лайм-бореліоз: сучасні схеми специфічної антибіотикотерапії
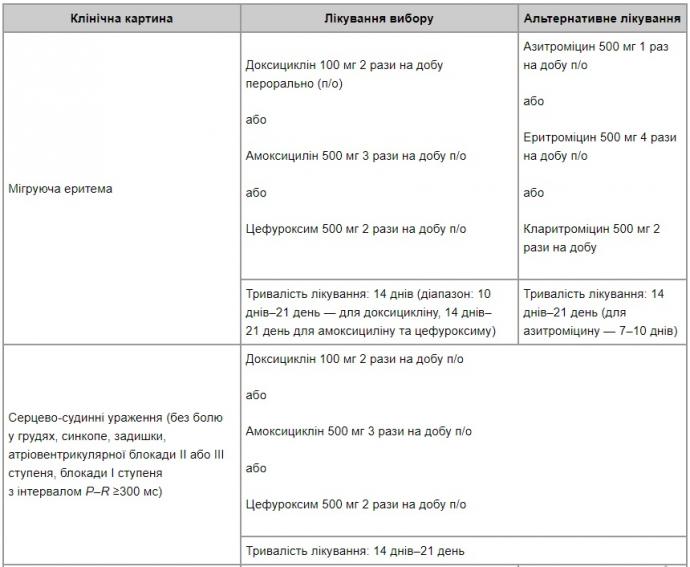
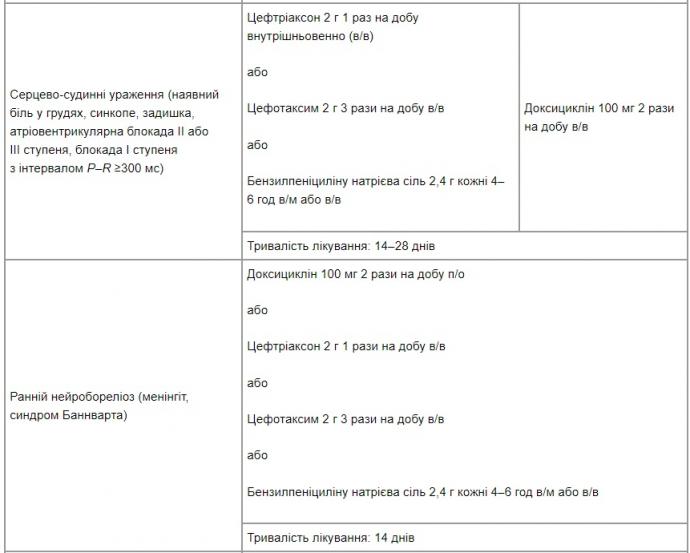
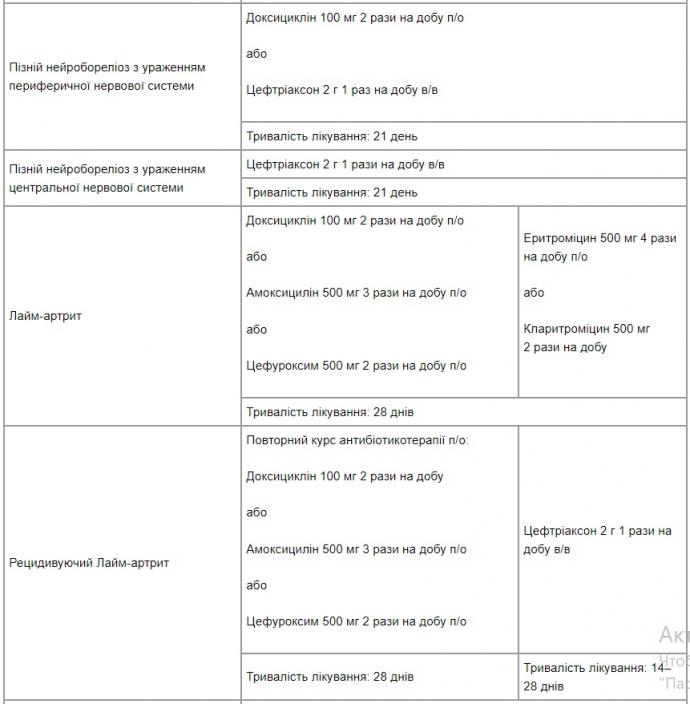
Лікування пацієнтів із Лайм-бореліозом полягає у проведенні специфічної антибіотикотерапії. У табл. 2 наведено схеми специфічної антибіотикотерапії при Лайм-бореліозі (для дорослих).
Таблиця 2. Лайм-бореліоз: специфічна антибіотикотерапія

Лайм-бореліоз: постконтактна профілактика
Згідно з рекомендаціями Центрів контролю та профілактики захворювань США (Centers for Disease Control and Prevention — CDC), постконтактну профілактику Лайм-бореліозу (прийом доксицикліну 200 мг перорально однократно) необхідно здійснювати у тому разі, якщо мають місце всі нижченаведені позиції:
- Наповнений кров’ю кліщ Ixodes scapularis видалений через ≥36 год після прикріплення.
- З моменту видалення кліща пройшло не більше 72 год.
- Поширеність B. burgdorferiу місцевих кліщів становить >20%;
- Немає протипоказань до застосування доксицикліну.
Важливо спостерігати за місцем укусу кліща протягом 1 міс та розпочати лікування у разі появи клінічних проявів Лайм-бореліозу.
Висновки
- Мігруюча еритема — патогномонічний симптом Лайм-бореліозу. Поява мігруючої еритеми при встановленому контакті з кліщем в ендемічній зоні є показанням до початку специфічної антибіотикотерапії та не потребує серологічного підтвердження.
- Серологічна діагностика Лайм-бореліозу повинна включати два етапи: ІФА та вестерн-блот. Сумнівні та позитивні результати ІФА мають бути підтвердженні дослідженням вестерн-блот, тоді як негативні результати ІФА у більшості випадків не потребують проведення подальших досліджень.
- Визначення синтезу інтратекальних антитіл є золотим стандартом діагностики нейробореліозу.
- Молекулярно-генетичне дослідження при Лайм-бореліозі (виявлення ДНК B. Burgdorferi) має найбільшу діагностичну цінність при дослідженні синовіальної рідини у пацієнтів із Лайм-артритом, у інших випадках чутливість ПЛР низька.
- Згідно з настановами ESCMID, дослідження кліщів на наявність антигенів або ДНК борелій не рекомендоване. Постконтактна профілактика Лайм-бореліозу після видалення кліща полягає в однократному прийомі доксицикліну у дозі 200 мг перорально та має проводитися за наявності показань.
Список використаної літератури
- ESCMID Study Group of Lyme Borreliosis (2013) (https://bit.ly/3dtsuxf).
- ILADS Lyme Disease Treatment Guidelines (2019) (https://bit.ly/2UnwmIt).
- Meyerhoff J.O. (2019) Lyme Disease. Medscape, May 9.
- NICE Lyme disease guideline (2018) (https://bit.ly/2UBBhEF).
- Nyman D., Wahlberg P. (2017) Lyme-Borreliose. Duodecim Medical Publications Ltd, Mar. 3.
- Wormser G.P., Dattwyler R.J., Shapiro E.D. et al. (2007) The clinical assessment, treatment, and prevention of lyme disease, human granulocytic anaplasmosis, and babesiosis: clinical practice guidelines by the Infectious. Dis. Soc. Amer., Oct.1.