Основные направления менеджмента фибрилляции предсердий
Основной целью настоящих обновлений стало внесение изменений в имеющиеся Рекомендации 2014 г., существенно влияющих на принятие решения относительно тактики лечения. Внесение дополнительных изменений касается назначения антикоагулянтных препаратов для профилактики эмболических осложнений, катетерной абляции для устранения фибрилляции предсердий (ФП), лечения пациентов с ФП на фоне острого коронарного синдрома (ОКС), а также рассмотрение показаний для хирургического размещения противоэмболических устройств для нефармакологической профилактики эмболических осложнений. Приведенные дополнения помогут существенно улучшить тактику лечения пациентов с ФП.
4.1.1. Профилактика тромбоэмболических осложнений (табл. 1). Выбор антикоагулянтного препарата (исходя из оценки соотношения риск/польза).
Таблица 1. Рекомендации выбора антикоагулянтного режима риск/польза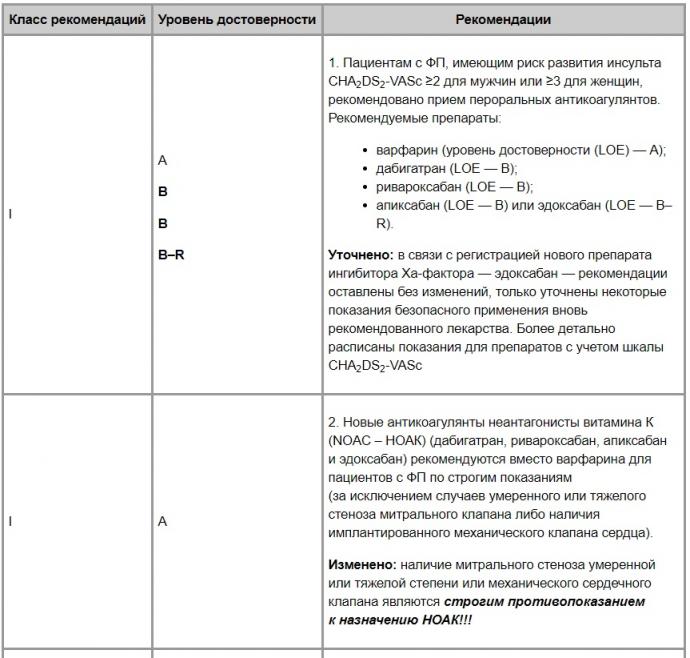
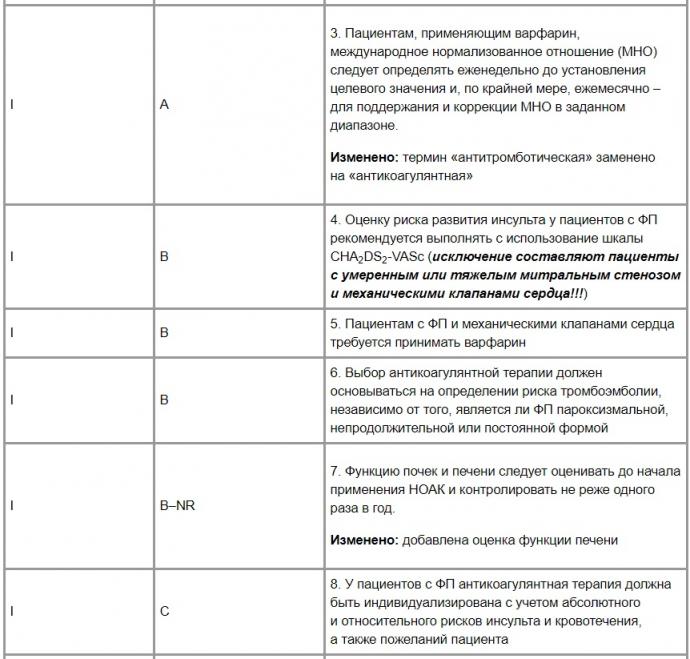
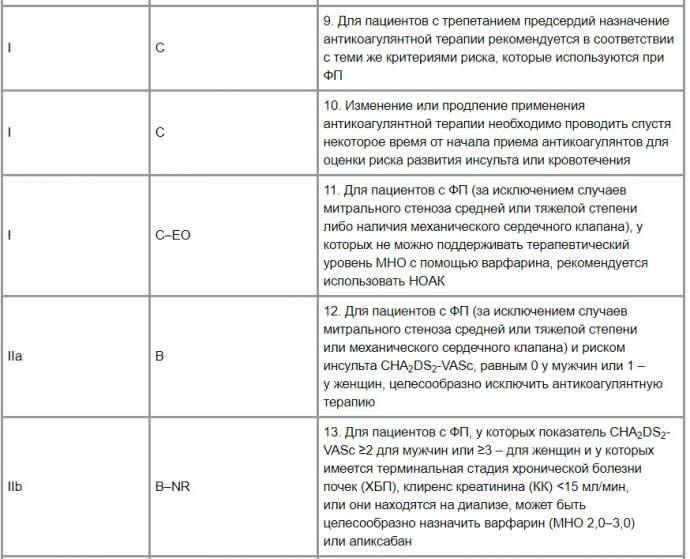
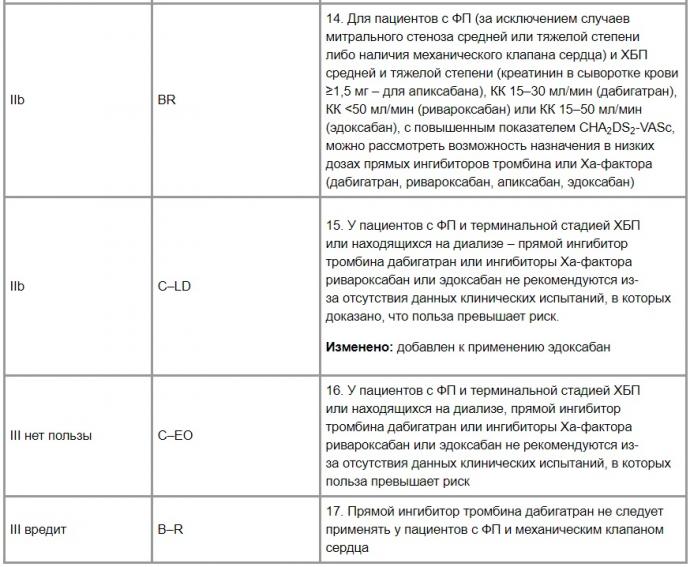
Разъяснения и уточнения по поводу принятых изменений
1. Доказано что применение эдоксабана в дозе 30–60 мг 1 раз в сутки не уступает по эффективности варфарину в отношении профилактики инсульта или системной эмболизации и имеет значительно более низкие показатели кровотечений и смертности от сердечно-сосудистых причин. Назначение эдоксабана в дозе 30 или 60 мг пациентам с ФП должно основываться на оценке риска инсульта и кровотечений. В исследовании ENGAGE-TIMI 48 выявлено, что частота системной эмболии и инсульта составляла 1,5% при применении варфарина и 1,2% — при приеме эдоксабана 60 мг (относительный риск (ОР) 0,79; 97,5% доверительный интервал (ДИ) 0,63–0,99; р<0,001) и 1,6% — при применении 30 мг эдоксабана (ОР 1,07; 97,5% ДИ 0,87–1,31; р=0,005). Частота серьезных кровотечений в группе варфарина составила 3,4% против 2,8% при применении 60 мг эдоксабана (ОР 0,80; 95% ДИ 0,71–0,91; р<0,001) и 1,6% — при 30 мг эдоксабана (ОР 0,47; 95% ДИ 0,41–0,55; р<0,001). В предшествующем Руководстве 2014 г. назначение пероральных антикоагулянтов требовалось при наличии инсульта в анамнезе, транзиторной ишемической атаки или CHA2DS2-VAS ≥2 баллов. В обновленных рекомендациях показания для назначения антикоагулянтной терапии определяются только на основании шкалы CHA2DS2-VASc. При этом антикоагулянтные препараты остались теми же.
2. По данным 4 рандомизированных исследований, сравнивающих НОАК с варфарином, доказано их сопоставимое влияние на риск развития инсульта или системной эмболии. При этом они сохраняли превосходный профиль безопасности и могут быть рекомендованы в качестве терапии первой линии для подходящих пациентов.
4. Рекомендация аналогична Руководству 2014 г. Появились новые данные, подчеркивающие существенные различия в разных группах пациентов с ФП, включая различные неевропейские популяции и общую частоту инсультов для данного балла CHA2DS2-VASc (S4.1.1-40). Опубликованы дополнительные подходы к прогнозированию риска инсульта и серьезных клинических исходов у отдельных пациентов с ФП, в том числе для специфического выбора антикоагулянта (S4.1.1-41–S4.1.1-42). Антикоагуляция при ФП и гипертрофической кардиомиопатии остается такой же, как в Руководстве 2014 г.
Пациенты с биопротезами сердечных клапанов не были включены в исследования с использованием критериев риска развития инсульта CHA2DS2-VASc. Что касается биопротезных клапанов, существует очень ограниченный опубликованный опыт использования системы оценки CHA2DS2-VASc для долгосрочной оценки риска тромбоэмболии у пациентов с ФП. В одном из отчетов установлено, что у пациентов с ФП увеличение возраста и повышение балла по шкале CHA2DS2-VASc были независимыми предикторами тромбоэмболических осложнений. У этих пациентов с ФП низкий показатель CHA2DS2-VASc был связан с низким риском тромбоэмболии независимо от того, имели ли пациенты биопротезные клапаны (S4.1.1-43). Кроме того, в исследованиях ARISTOTLE (апиксабан) и AFAGE TIMI 48 (эдоксабан) количество пациентов с ФП (с механическим протезом митропального или биопротезом аортального клапана) было небольшим, что затрудняет правильную оценку результатов. В этих небольших подгруппах результаты показали, что апиксабан (41 пациент) и эдоксабан (191 пациент), по-видимому, являются возможной альтернативой варфарину у пациентов с ФП и одним имплантированным биопротезом клапана. Несмотря на стандартную практику применения антикоагулянтной терапии при биопротезировании коротким непродолжительным курсом, для рутинного долгосрочного ее применения необходимы дальнейшие исследования. На сегодня шкала CHA2DS2-VASc может быть рекомендована пациентам с ФП и биопротезами клапанов сердца для назначения антикоагулянтов.
5. Имплантация одного механического клапана и только в аортальную позицию имеет одобренные Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (Food and Drug Administration — FDA) рекомендации по поддержанию МНО 1,5–2,0 (спустя 3 мес после имплантации) при применении варфарина и ацетилсалициловой кислоты в низких дозах. Исследование с участием небольшой группы пациентов проведено для проверки того, является ли безопасным и эффективным менее агрессивная антикоагулянтная терапия пациентов после имплантации клапаном On-X. В исследование были включены также пациенты с ФП, которым имплантировали аортальный протез.
7. Все 4 НОАК, одобренные FDA для применения у пациентов с ФП, имеют дозировку, определяемую почечной функцией (уровень креатинина или КК по Кокрофту — Голту). При назначении апиксабана необходима коррекция дозы с учетом возраста (≥80 лет) или массы тела (≤60 кг). Эдоксабан не одобрен для применения у пациентов с нарушенной функцией почек (КК <30 мл/мин) или верхней границей почечной функции (КК >95 мл/мин). Почечная функция должна регулярно контролироваться, а КК — рассчитываться с интервалом, который зависит от индивидуальной степени почечной дисфункции и задержки жидкости, а коррекцию дозы необходимо производить в соответствии с рекомендациями FDA. Кроме того, для ингибиторов Xa-фактора следует периодически контролировать функцию печени. НОАК не рекомендуется для применения у пациентов с тяжелой печеночной дисфункцией.
12. Многие факторы риска способствуют повышению риска инсульта у пациентов с ФП, что выражается в баллах CHA2DS2-VASc. Доказательства того, что женский пол является фактором риска, оценивались во многих исследованиях. Большинство исследований подтверждают, что женщины с ФП подвержены повышенному риску инсульта. Один метаанализ показал, что в 1,31 раза (95% ДИ 1,18–1,46) повышен риск развития инсульта у женщин с ФП, при этом риск больше всего проявляется у женщин в возрасте ≥75 лет. Недавние исследования показали, что у женского пола, в отсутствие других факторов риска ФП (CHA2DS2-VASc 0 баллов — для мужчин и 1 балл — для женщин), отмечен низкий риск инсульта и аналогичен такому у мужчин. Чрезмерный риск для женщин был особенно очевиден среди лиц с ≥2 факторами риска инсульта, не связанными с полом. Таким образом, женский пол является предиктором риска и зависит от возраста. Добавление женского пола к баллу CHA2DS2-VASc имеет значение для возраста >65 лет или ≥2 баллов риска инсульта, не связанных с полом.
13. Пациенты с терминальной стадией ХБП, находящиеся на диализе, имеют высокую распространенность ФП, других связанных факторов риска инсульта и повышенный риск кровотечения. Установлено, что варфарин, изученный в крупных ретроспективных исследованиях, обеспечивает защиту от сердечно-сосудистых событий без повышения риска кровотечения; однако в недавнем метаанализе выявлено, что варфарин не способствовал снижению смертности, частоте ишемических событий или инсультов, но повышал частоту развития опасных кровотечений.
Существуют ограниченные данные о применении апиксабана в одной или нескольких дозах (2,5 или 5 мг) у пациентов с ФП и ХБП, находящихся на диализе, по сравнению со здоровыми участниками исследования. У пациентов с ХБП на диализе накапливается апиксабан (повышение концентрации в плазме крови) при приеме 2,5 мг 2 раза в сутки, что приводит к устойчивому воздействию препарата, сопоставимому с 5 мг 2 раза в сутки ежедневно у пациентов с сохраненной функцией почек.
Диализ оказывал ограниченное влияние на клиренс апиксабана. Частота таких осложнений, как кровотечение, была уменьшена при снижении дозы апиксабана. В недавнем исследовании сравнивали апиксабан (5 мг против 2,5 мг 2 раза в сутки) и варфарин у диализзависимых пациентов с ФП. Пациенты, применявшие апиксабан в стандартной дозе (5 мг), имели более низкий риск развития инсульта/эмболии, чем лица, получавшие в низких дозах апиксабан (2,5 мг) и варфарин. Апиксабан в стандартной дозе ассоциировался с более низким риском смерти, а также развития сильного кровотечения, чем в случае применения апиксабана и варфарина в низких дозах (S4.1.1-30). Использование варфарина или апиксабана может быть целесообразным у диализзависимых пациентов с ФП, но требуется проведение дальнейших исследований.
14. Эдоксабан (30 или 60 мг 1 раз в сутки) изучали в исследовании ENGAGE AF-TIMI 48. Установлено, что препарат не уступает варфарину в отношении профилактики инсульта или системной эмболизации и связан со значительно более низкими показателями кровотечений и смертности от сердечно-сосудистых причин (S4.1.1-11).
15. Существует неопределенность в отношении того, оправдана ли антикоагуляция у мужчин и женщин с ФП с баллом CHA2DS2-VASc, равным 1 или 2 соответственно. Женщины с ФП, вероятно, старшего возраста имеют повышенный риск развития инсульта (S4.1.1-31–S4.1.1-33). Однако женский пол сам по себе не несет повышенного риска в отсутствие других факторов (S4.1.1-34, S4.1.1-35, S4.1.1-58). Недавние исследования большой когорты пациентов с ФП касались изучения преимуществ антикоагуляции среди пациентов, имевших 1 фактор риска, не связанный с полом (CHA2DS2-VASc 1 — у мужчин и 2 — у женщин) (S4.1.1-58). Авторы выявили, что пациенты, не получавшие антикоагулянты, имевшие 1 фактор риска инсульта, не связанный с полом (CHA2DS2-VASc (1 против 0 — у мужчин и 2 против 1 — у женщин), имели повышенный риск серьезных сердечно-сосудистых событий во время наблюдения. Важно отметить, что применение антикоагулянта варфарина было связано с небольшой положительной клинической выгодой (измеряемой как снижение частоты ишемического инсульта, в то же время — незначительным увеличением внутричерепного кровоизлияния) по сравнению с теми, кто его не принимал. Подобные исследования необходимы также и для изучения НОАК.
16. Эдоксабан до 50% из организма выделяется почками. Прием рекомендован 1 раз в сутки. Не рекомендуется назначать препарат пациентам с терминальной стадией почечной недостаточности или находящимся на хроническом диализе (S4.1.1-11). Имеются публикации, содержащие ограниченные данные по фармакокинетике разовой дозы ривароксабана у пациентов с терминальной стадией заболевания почек, находящихся на диализе (S4.1.1-59, S4.1.1-60). Установлено, что применение дабигатрана и ривароксабана сопровождалось более высоким риском госпитализации или смерти от кровотечений, чем при применении варфарина (S4.1.1-61).
17. Исследование RE-ALIGN (рандомизированное исследование II фазы для оценки безопасности и фармакокинетики перорального дабигатрана у пациентов после замены сердечного клапана) представляло собой многоцентровое проспективное рандомизированное исследование II фазы по оценке дабигатрана в сравнении с варфарином, в которое были включены пациенты в возрасте 18–75 лет следующих состояний: замена клапана сердца механическим протезом в аортальной или митральной позиции (или обоих) в течение предшествующих 7 дней (группа А) или замена только митрального клапана механическим протезом (с/без замены аортального клапана) более чем за 3 мес до рандомизации (группа B). Исследование было остановлено после того, как в него вошли 252 пациента, из-за неприемлемо высоких показателей тромбоэмболии и кровотечений в группе дабигатрана. Аналогичная информация о безопасности и эффективности антикоагулянтной терапии с применением ривароксабана, апиксабана и эдоксабана у пациентов после протезирования клапанов сердца отсутствует.
4.2. Выбор антикоагулянта (изменения в пункте 4.2 «антитромботические средства»)
4.2.2.2. Пероральные антикоагулянты, не влияющие на витамин K (изменено в пункте 4.2.2.2, вместо «Новые целевые пероральные антикоагулянты» в Руководстве 2014 г.)
Большинство НОАК, применяющихся для предупреждения развития тромбоэмболических осложнений или инсульта, по сравнению с варфарином обладают большей безопасностью и являются несомненным достижением в области антикоагуляции последних лет у пациентов с ФП. Во многочисленных исследованиях доказано, что НОАК при ФП не уступают и даже превосходят варфарин в предотвращении инсульта или тромбоэмболических осложнений, а также имеют значительно более низкую частоту развития внутричерепных геморрагий по сравнению с варфарином. И хотя данных больших рандомизированных исследований по сравнению безопасности и эффективности препаратов между собой мало, все же их достаточно для некоторых заключений. Так, применение апиксабана может иметь более низкий риск развития кровотечения (включая внутричерепное кровоизлияние) и повышенную эффективность для профилактики инсульта, тогда как риск кровотечения для ривароксабана сопоставим с риском приема варфарина. Также показано, что длительное применение дабигатрана имело более благоприятный исход, чем прием варфарина, при выполнении радиочастотной абляции при ФП (исследование RE-CIRCUIT). Длительный прием НОАК (особенно дабигатрана и ривароксабана), вероятно, имеет более низкий риск развития формирования почечной патологии, чем варфарин. Прием НОАК лицами пожилого возраста сопровождался более низкой частотой развития остеопороза и патологических переломов костей (особенно это касается дабигатрана) по сравнению с применявшими варфарин.
В то же время существующая на сегодня система контроля уровня концентрации НОАК у конкретного пациента не всегда выполнима, а ее клиническая эффективность требует дальнейшего совершенствования. Поэтому на сегодня соответствующие анализы проводят в ситуациях, сопряженных с риском развития кровотечения, коррекции дозы для повышения эффективности лечения или снижения токсичности препарата и включают следующие состояния:
- Надобность экстренного хирургического вмешательства у пациентов, применяющих НОАК.
- Пациенты, находящиеся на диализе или имеющие ХБП с подозреваемым токсическим накоплением НОАК в сыворотке крови.
- С целью коррекции дозы НОАК для уменьшения патологического лекарственного взаимодействия.
- Оценка всасывания лекарств у пациентов с тяжелым ожирением (индекс массы тела >35 или масса тела >120 кг).
- Оценка приверженности пациента лечению.
4.3. Условия прекращения применения НОАК и перевод пациента на другие антикоагулянтные препараты
Разъяснения и уточнения по поводу принятых изменений
2. В исследовании BRIDGE установлено, что пациенты с ФП, которым потребовалась временная отмена приема варфарина в связи с клинической ситуацией (за исключением пациентов со стенозом митрального клапана средней и тяжелой степени и механическим клапаном сердца) как с бриджинг-терапией низкомолекулярным гепарином (табл. 2), так и без нее, имели одинаково низкий риск развития неблагоприятных осложнений — кровотечений и тромбоэмболий. Бриджинг-терапию следует рассматривать только у тех пациентов, у которых прекращение приема варфарина сопровождается крайне высоким риском тромбоэмболических осложнений!
Таблица 2. Рекомендации по мостовидной терапии (бриджинг-терапия) при прекращении приема пероральных антикоагулянтов и продолжении антикоагулянтной терапии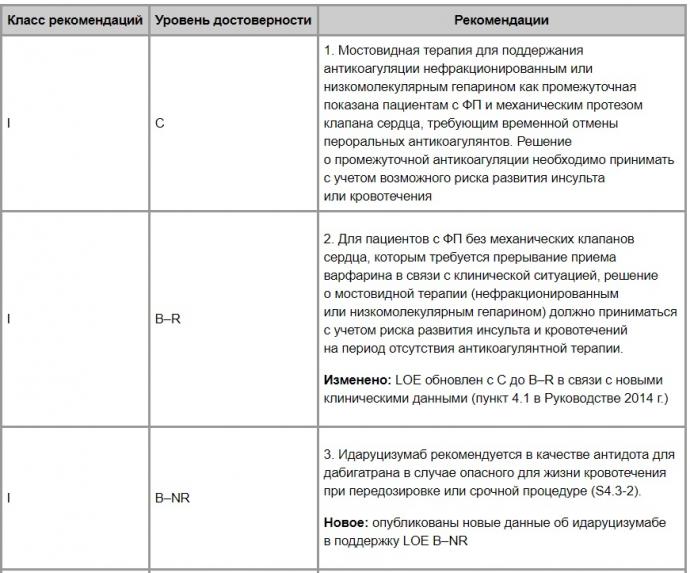

3. Действие антидота идаруцизумаба, созданного на базе моноклональных антител к дабигатрану, изучали в исследовании RE-VERSE AD. Установлено что идаруцизумаб способен необратимо связываться с дабигатраном и быстро восстанавливать гемостаз за счет снижения уровня, циркулирующего дабигатрана в крови. Также выявлено, что в случаях развития серьезного кровотечения или при необходимости экстренного вмешательства с риском кровотечения препарат оказался очень эффективным. В связи с этим идаруцизумаб получил одобрение FDA как антидот дабигатрана.
4. Андексанет альфа — рекомбинантный белковый препарат, инактиватор Xa-фактора. Препарат получил одобрение FDA после успешного испытания с участием добровольцев в качестве антидота против прямых ингибиторов Xa-фактора. Результаты получены в испытаниях с участием добровольцев, применявших ривароксабан и апиксабан. И хотя одобрение FDA получено, требуются более масштабные клинические исследования для уточнения его влияния на гемостаз у пациентов в реальных клинических ситуациях.
4.4. Нефармакологические пути профилактики развития инсульта
4.4.1. Малоинвазивное размещение окклюдера в ушке левого предсердия (УЛП) (табл. 3)
Таблица 3. Рекомендации по интервенционному закрытию УЛП (ссылки на исследования, одобряющие новые рекомендации, обобщены в пункте 4 в онлайн-версии)
Разъяснения и уточнения по поводу принятых изменений
Сравнительный анализ эффективности чрескожной окклюзии УЛП окклюдером Watchman и применения варфарина у пациентов с ФП (при отсутствии митрального стеноза средней или тяжелой степени и без механического клапана сердца) при повышенном риске инсульта, проведенный в двух исследованиях PROTECT AF и PREVAIL, показал, что у пациентов с размещенным устройством частота геморрагического инсульта была ниже, чем у принимавших варфарин. Но наблюдалась более высокая частота развития ишемического инсульта (S4.4.1-3). Однако после устранения перипроцедурных недочетов эта разница была статистически недостоверной.
Таким образом, пероральная антикоагуляция остается предпочтительной терапией для профилактики инсульта у большинства пациентов с ФП и повышенным риском инсульта. Тем не менее для пациентов, являющихся неподходящими кандидатами на длительную пероральную антикоагуляцию (из-за склонности к кровотечению или плохой лекарственной переносимости и низкой приверженности лечению), малоинвазивное закрытие УЛП окклюдером Watchman может рассматриваться как метод выбора.
Существуют важные различия в формулировках показаний малоинвазивного закрытия УЛП от FDA и Centers for Medicare & Medicaid Services (CMS). В рекомендациях FDA устройство рекомендовано как альтернативная процедура для пациентов, которые считались подходящими для длительного приема варфарина, но имелась соответствующая потребность поиска нефармакологической альтернативы варфарину. Наоборот, CMS предлагает применять устройство в качестве альтернативы для пациентов, которые не могут быть кандидатами для длительного приема варфарина. При этом основным критерием назначения процедуры служит величина риска по шкале CHADS2 ≥2 баллов и CHA2DS2-VASc ≥3 баллов. Остается ряд нерешенных вопросов, в том числе оптимальный отбор пациентов и перипроцедурная антитромботическая схема профилактики осложнений. Текущие рекомендации FDA гласят, что пациенты должны считаться подходящими для антикоагуляции, в том числе и в перипроцедурный период. Пациенты, которые не способны принимать пероральную антикоагулянтную терапию, в исследование по тестированию Watchman не включались. В то же время за пределами США наблюдается растущий опыт закрытия УЛП у пациентов, которым назначали исключительно только антиагрегантные препараты.
4.4.2. Кардиохирургическое закрытие УЛП
Разъяснения и уточнения для корректного принятия решения
Получены новые данные в поддержку хирургической окклюзии УЛП у пациентов с ФП в анамнезе (табл. 4). В обсервационном исследовании оценена связь между хирургической окклюзией УЛП (обычно с хирургической абляцией предсердий), проводимой одновременно с операциями на сердце у пациентов пожилого возраста с ФП в анамнезе и риском послеоперационных тромбоэмболических осложнений (S4.4.2-1). Авторы использовали информацию о пациентах из реестра базы данных кардиохирургических исследований Общества торакальных хирургов, которая содержит периоперационную информацию о краткосрочных (в течение 30 дней) исходах. Исследование связало информацию о пациентах из базы данных Общества кардиохирургических вмешательств Общества торакальных хирургов с данными Medicare (возраст ≥65 лет) и частотой повторной госпитализации в течение 3 лет после операции по поводу тромбоэмболии (инсульт, транзиторная ишемическая атака или системная эмболия). В исследования включены результаты лечения 10 524 пациентов, перенесших хирургические операции на сердце, в том числе 3892 (37%) пациента с хирургической окклюзией УЛП. При среднем периоде наблюдения 2,6 года хирургическая окклюзия УЛП по сравнению с отсутствием окклюзии УЛП была связана с более низкими нескорригированными показателями госпитализации в связи с тромбоэмболией (4,2% против 6,2%), смертности от всех причин (17,3% против 23,9%) и комбинированной конечной точки (20,5% против 28,7%). Существенной разницы в показателях частоты геморрагического инсульта не было (0,9% в обеих группах). Эти данные свидетельствуют о том, что хирургическая окклюзия УЛП может быть связана с уменьшением послеоперационных тромбоэмболических осложнений у пациентов пожилого возраста с ФП.
Таблица 4. Рекомендации по кардиохирургическому закрытию УЛП (исследование, посвященное окклюзии/иссечению, поддерживает обновленную рекомендацию в пункте 5 в онлайн-версии)
Анализ в подгруппах, стратифицированных по качеству антикоагуляции при выписке из стационара среди пациентов с ФП в анамнезе, которым была выполнена окклюзия УЛП без послеоперационной антикоагуляции, свидетельствует о значительно более низкой частоте тромбоэмболии, нежели у тех, кому процедуру не проводили и не назначали антикоагулянтные препараты. Не выявлено также различий в риске тромбоэмболии среди пациентов с ФП, получавших антикоагулянтные препараты независимо от того, выполнялась ли окклюзия УЛП. Что подтверждает значимость антикоагулянтной терапии в профилактике эмболии у пациентов с ФП независимо от окклюзии УЛП. Сравнительный анализ профилактической хирургической окклюзии УЛП у пациентов, перенесших операцию на сердце, не продемонстрировал связи между окклюзией УЛП и снижением частоты тромбоэмболических осложнений в отдаленной перспективе. В то же время пациенты, имевшие ФП в анамнезе и которым выполнена окклюзия УЛП без устранения нарушения ритма, имели высокую частоту возврата ФП, но это не влияло на повышение риска развития инсульта или смерти.
6. Контроль сердечного ритма
6.1. Электрическая и фармакологическая кардиоверсия при ФП и трепетании
6.1.1. Рекомендации по профилактике тромбоэмболии. Обновленные рекомендации, пункт 6 онлайн-версии (табл. 5)
Таблица 5. Рекомендации по профилактике тромбоэмболии (обновленные рекомендации, пункт 6 онлайн-версии)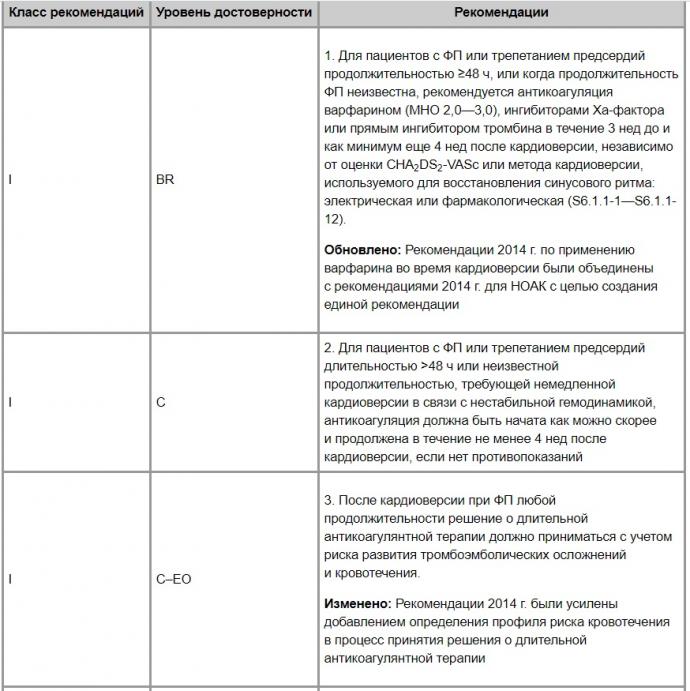
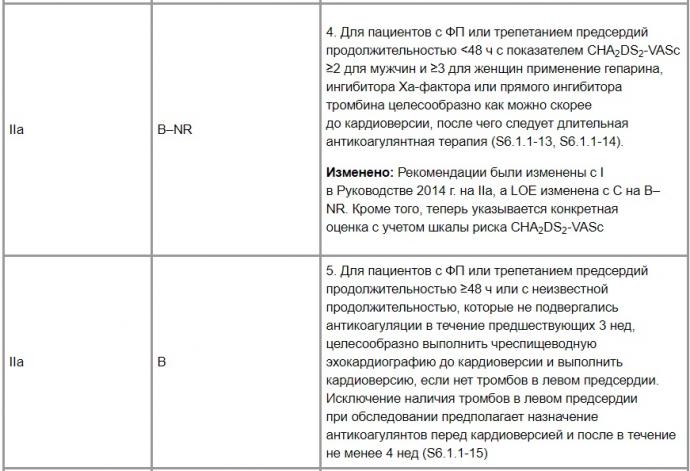

1. Оценка эффективности и безопасности недавнего применения ингибиторов Ха-фактора (ривароксабан и апиксабан) при кардиоверсии в качестве альтернативы варфарину проведена в нескольких рандомизированных клинических исследованиях (S6.1.1-7, S6.1.1-8, S6.1.1-17). Кроме того, проведен ретроспективный анализ подгруппы пациентов, перенесших кардиоверсию, где сравнивался каждый из одобренных FDA НОАК с варфарином для профилактики тромбоэмболии у пациентов с ФП. В результате проведенных исследований подтверждено, что НОАК являются эффективной и безопасной альтернативой варфарину для пациентов, которым требовалась кардиоверсия. Чреспищеводную эхокардиографию можно рассматривать как альтернативный диагностический подход для пациентов, ожидающих более 3 нед кардиоверсии, с целью исключения тромбоза левого предсердия. Решение о долгосрочной антикоагулянтной терапии (более 4 нед) основывается на профиле тромбоэмболического риска (раздел 4) и профиле риска кровотечения. «Правило 48 часов» также подвергалось изменению, поскольку задержка кардиоверсии более 12 ч с момента появления симптомов была связана с более высоким риском тромбоэмболических осложнений по сравнению с кардиоверсией, выполненной в пределах 12 ч (1,1 и 0,3% соответственно) (S6.1.1-18). При этом риск тромбоэмболических осложнений у пациентов в возрасте старше 75 лет и у женщин при кардиоверсии, выполненной спустя 12 ч, значительно повышается (S6.1.1-19).
4. Данные, подтверждающие безопасность современной практики проведения кардиоверсии при ФП без пероральной антикоагуляции у пациентов с длительностью ФП <48 ч, ограничены. Два недавних ретроспективных исследования подтвердили, что риск тромбоэмболических осложнений кардиоверсии при ФП продолжительностью <48 ч находится в диапазоне от 0,7 до 1,1%. При этом более высокий риск сохраняется у пациентов женского пола, а также у лиц с сохраняющейся сердечной недостаточностью и сахарным диабетом. Также сделана оговорка, что пациенты в возрасте младше 60 лет без тромбоэмболических факторов риска и лица с послеоперационной ФП, по-видимому, имеют более низкий риск тромбоэмболий (S6.1.1-13, S6.1.1-14). В одном из исследований (567 кардиоверсий у 484 пациентов) установлено, что риск тромбоэмболии был почти в 5 раз выше у пациентов, не получавших антикоагулянтной профилактики в терапевтических пределах, по сравнению с теми, кто принимал варфарин или гепарин (S6.1.1-14). И все же вне зависимости от результатов полученных исследований при назначении антикоагулянтной терапии риск тромбоэмболических осложнений следует сопоставить с риском связанного с приемом антикоагулянта кровотечения для конкретного пациента.
6.3. Катетерная абляция при ФП для восстановления синусового ритма
6.3.4. Катетерная абляция при сердечной недостаточности(табл. 6)
Таблица 6. Рекомендации по катетерной абляции пациентов с сердечной недостаточностью (обновленные рекомендации пункта 7 в онлайн-дополнении)
В группе катетерной абляции при ФП по сравнению с группой контроля выявлено значительное снижение смертности, частоты госпитализации по поводу нарастания сердечной недостаточности и повышение фракции выброса левого желудочка по сравнению с группой медикаментозной терапии. При этом была намного выше частота восстановления синусового ритма. Также получена более высокая частота восстановления сердечного ритма по сравнению с применением амиодарона и другими аппаратными методиками, а анализ вторичных точек выявил более низкую частоту незапланированных госпитализаций и внезапной смерти (S6.3.4-2). Отметим, что данные исследований имеют ограничение в трактовке результатов, поскольку группы пациентов были сформированы с хорошо подобранными параметрами.
В анализе результатов, сравнивающих абляцию при ФП с медикаментозным восстановлением ритма у пациентов с сердечной недостаточностью и низкой фракцией выброса, также выявлены лучшие результаты в группе пациентов, которым проводили абляцию. Продемонстрировано повышение частоты восстановления синусового ритма, толерантности к физической нагрузке при выполнении теста с 6-минутной ходьбой, а также повышение фракции выброса левого желудочка и улучшение качества жизни. (S6.3.4-3, S6.3.4-4). Однако недавнее исследование CABANA показало, что абляция при ФП не превосходит медикаментозную терапию по первичным сердечно-сосудистым исходам и частоте внезапной смерти, инсульта, серьезных кровотечений на протяжении 5 лет среди пациентов с недавно возникшей или нелеченной ФП (S6.3.4-5, S6.3.4-6).
7. Особые группы пациентов с ФП7.4. ФП как осложнение ОКС(табл. 7)
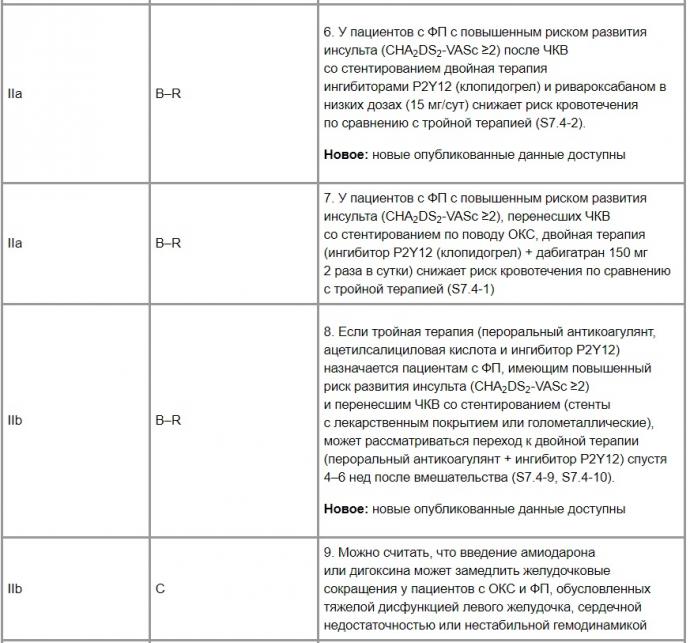
Таблица 7. Рекомендации оказания помощи при ФП у пациентов с ОКС (онлайн-дополнение к пункту 8)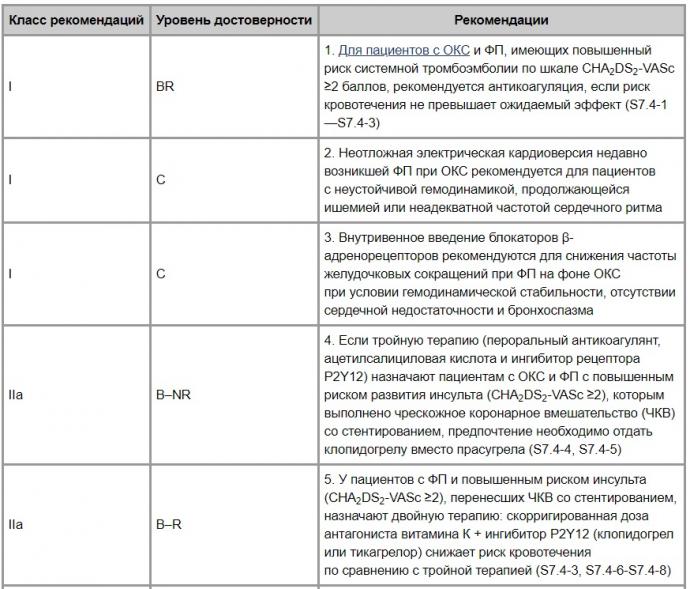

- January C.T., Wann L.S., Calkins H. et al.(2019) 2019 AHA/ACC/HRS Focused Update of the 2014 AHA/ACC/HRS Guideline for the Management of Patients With Atrial Fibrillation. Heart Rhythm, S1547–5271(19)30037-2. doi: https://doi.org/10.1016/j.hrthm.2019.01.024.