ESMO Clinical Practice Guidelines 2018
Захворюваність та епідеміологія
Частота захворювання на лімфому Ходжкіна (ЛХ) у Європейському Союзі становить 2.3 випадків, а смертність 0,4 випадки / 100 000 населення / рік.
Найчастіше хворіють молоді люди у віці 20-40 років. Чоловіки хворіють частіше. Гістологічно виділяють
класичну форму ЛХ (кЛХ), яка зустрічається у 95% випадків, що відрізняється від нодулярної форми з переважанням лімфоцитів (НФПЛЛХ), яка складає 5 % усіх випадків ЛХ.
Діагоностика
Діагностика повинна проводитися відповідно до класифікаціЇ ВООЗ використовуючи ексцизійну біопсію лімфатичних вузлів або хірургічний зразок, щоб забезпечити достатню кількість матеріалу для виготовлення свіжозаморожених та фіксованих формаліном зразків. Виявлення у зразку клітин Березовського-Ріда-Штернберга свідчить про кХЛ, тоді як виявлення переважно лімфоцитів свідчить про НФПЛЛХ. Імунофенотип злоякісних клітин при кХЛ і НФПЛЛХ значно відрізняється.
Визначення та оцінка ризиків
Для діагностики необхідно враховувати: анамнез хвороби, включаючи симптоми B (лихоманку, нічну пітливість, незрозумілу втрату ваги > 10% протягом 6 місяців), інші загальні симптоми пов'язані з хворобою (надмірну втомлюваність, свербіж), можливу наявність болю у лімфовузлах після вживання алкоголю, а також
результати фізикального огляду. Рентген грудної клітки та комп'ютерна томографія, КТ з контрастуванням (шиї, судин та черевної порожнини) є обов'язковими. Крім того, за можливості, слід провести позитронну емісійну томографію (ПЕТ) відповідно до рекомендацій щодо діагностики та оцінки лімфоми.
Враховуючи високу чутливість діагностики з ПЕТ-КТ при ураженні кісткового мозку, біопсію КМ пацієнтам, що пройшли оцінку ПЕТ-КТ можна не проводити [III, B].
Однак біопсія кісткового мозку повинна бути проведена, якщо проведення ПЕТ-КТ неможливе. Загальний аналіз крові, швидкість осідання еритроцитів (ШОЕ), біохімічний аналіз крові, включаючи С-реактивний білок, лужну фосфатазу лактатдегідрогеназу, печінкові проби та альбумін є обов'язковими. Скринінги на гепатит B (HBV), гепатит С (ВГС) та вірус імунодефіциту людини(ВІЛ) є обов'язковим [II-III, A].
Встановлення діагнозу проводиться відповідно до класифікації Ann Arbor з урахуванням визначених клінічних факторів ризику. Після встановлення діагнозу визначається одна з трьох стадій (обмежена, проміжна та поширена стадія) [II-III, A] .
Для виявлення пацієнтів з підвищеним ризиком гострих та / або відстрочених ускладнень та генерації вихідних значень для майбутніх вимірювань необхідно провести аналіз серцевої та легеневої функцій до початку лікування. Враховуючи те, що хіміотерапія і променева терапія абдомінальної ділянки може викликати безпліддя, пацієнтам репродуктивного віку до лікування
слід надавати консультування з приводу репродуктивної функції та висувати на розгляд питання про забір сперматозоїдів, ооцитів або кріоконсервації тканин яєчників.
Лікування кХЛ
Обмежена стадія хвороби
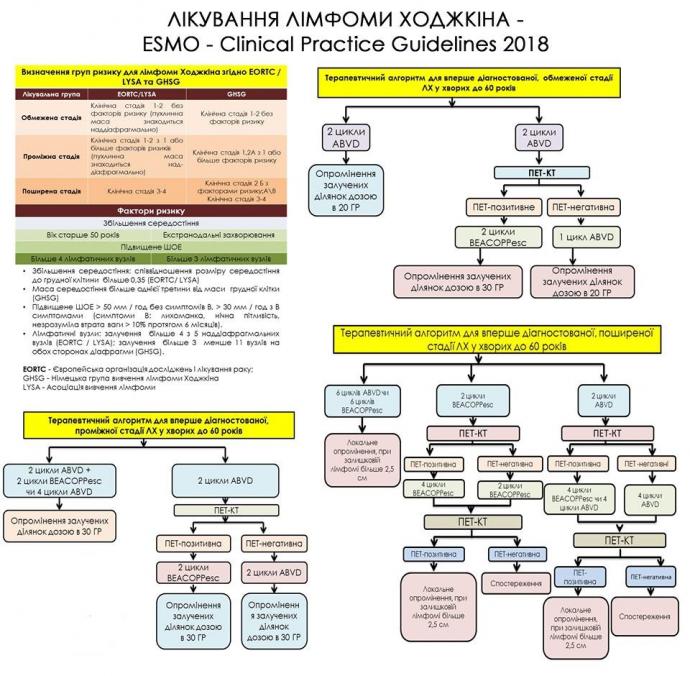
Показано, що застосування комбінованого лікування, яке складається з короткого курсу хіміотерапії та променевої терапії призводить до кращого зменшення пухлиної маси в порівнянні з застосуванням лише променевої терапії [I, A]. Два-три цикли доксорубіцину / блеоміцину / вінблістину /дакарбазину (ABVD) (табл. 3), після чого традиційно використовують променеву терапію являє собою стандарт медичної допомоги для обмеженої стадії ЛХ.
Найменш токсична схема складається з двох циклів ABVD з наступним опромінення 20 Гр і є достатнім для обмеженої стадії ЛХ [I, A].
Проводили порівняльний контроль у рандомізованому дослідженні, в якому порівнювались пацієнти, яким проводили променеву терапію у дозах 20 або 36 Гр і досягали повної ремісії після шести циклів хіміотерапії: епірубіцину / блеоміцину / вінбластину / преднізону (EBVP). Впродовж останніх років було проведено
декілька рандомізованих досліджень, присвячених цій проблемі. На основі даних було відмічено підвищення виживання без прогресування хвороби у пацієнтів, які отримували комбіноване лікування, незважаючи на проміжні негативні результати ПЕТ.
Таким чином, група пацієнтів, яка може отримувати лікування тільки у вигляді хіміотерапії, ще не може бути визначеною. [I, A]
Чим раніше розпочати лікування, тим кращий буде прогноз у пацієнтів з позитивним проміжним результатами ПЕТ.
Під час великого рандомізованого дослідження, що включало пацієнтів з обмеженою та проміжною стадією ЛХ, виявили значно знижений показник рецидиву у пацієнтів з позитивним проміжним результатом ПЕТ після двох циклів (ABVD), які пройшли хіміотерапію
з двома циклами блеоміцину /етопозиду / доксорубіцину / циклофосфаміду / вінкрістину / прокарбазину / преднізолону (BEACOPP) у збільшеній дозі, замість одного (при обмеженій стадії), або двох (при проміжній стадії) додаткових циклів перед ABVD до опромінення залученого лімфатичного вузла.
Проте дослідження не забезпечувало аналізу пацієнтів з обмеженою та проміжною стадіями хвороби окремо.
Пацієнтам з позитивними проміжними результатами ПЕТ після двох циклів ABVD слід призначати два цикли BEACOPP у збільшеній дозі перед місцевим опроміненням [I, A].
Проміжна стадія захворювання
Проміжна стадія ЛХ зазвичай лікується комібнованими методами. Чотири цикли ABVD, з наступним використанням фракціонованої променевої терапії у дозі 30 Гр вважається стандартом лікування ЛХ на проміжній стадії [I, A]. Для пацієнтів віком менше 60 років, які мають потребують більш інтенсивного лікування, цей стандарт оскаржується протоколом, що складається з двох циклів BEACOPP у збільшеній дозі, після цього два цикли ABVD і променева терапія у дозі 30 Гр. Підвищення загальної виживаності не вдалося відмітити [I, B-C].
За рекомендаціями Міжнародної групи з променевої терапії лімфоми краще після хіміотерапії застосовувати місцеве опромінення, ніж опромінення залучених ділянок. Під час великого рандомізованого дослідження не виявили переваги комплексного лікування над застосуванням лише хіміотерапії у пацієнтів з негативним проміжним ПЕТ [I, A].
Чим лікування було розпочато раніше, тим кращий прогноз у пацієнтів з проміжними позитивними результатами ПЕТ. Під час рандомізованого дослідження, яке включало хворих на ЛХ з обмеженою та проміжною стадією було виявлено значно зменшену частоту рецидивів у пацієнтів з позитивними проміжними результатами ПЕТ після двох циклів ABVD, які пройшли хіміотерапію з двома циклами блеоміцину /етопозиду / доксорубіцину / циклофосфаміду / вінкрістину / прокарбазину / преднізолону (BEACOPP) у збільшеній дозі, замість одного (при обмеженій стадії),
або двох (при проміжній стадії) додаткових циклів перед схемою ABVD та до опромінення залученого лімфатичного вузла.
Пацієнтам з позитивними проміжними результатами ПЕТ після двох циклів ABVD слід призначати два цикли BEACOPP у збільшеній дозі перед місцевим опроміненням [I, A].
У літніх людей, що приймають більше двох циклів ABVD може виникнути блеоміцин-індуковане отруєння, тому пацієнтам старше 60 років потрібно відміняти блеоміцин після другого циклу хіміотерапії [III, B – C].
Поширена стадія
Поширена стадія ЛХ зазвичай лікується тільки хіміотерапією. Додатково застосовується променева терапія у пацієнтів із залишковими явищами після хіміотерапії. Пацієнти віком менше 60 років лікуються або за схемою ABVD (шість циклів), або BEACOPP у
збільшеній дозі (від чотирьох до шести циклів), потім (не обов’язково) можна застосувати локальну променеву терапію [I, A].
Коли застосування циклів ABVD є неможливим, можна виключити блеоміцин, тобто застосовувати доксорубіцин/ вінбластин / дакарбазин (AVD) у вигляді 3-6 циклів при негативних проміжних результатах ПЕТ після двох циклів хіміотерапії; дану схему слід
розглядати, особливо у літніх пацієнтів в зв’язку з підвищеним ризиком токсичного впливу на легені [I, A].
Немає рандомізованого дослідження, що оцінює роль раннього лікування у хворих з поширеною стадією, які мають позитивні проміжні результати ПЕТ після двох циклів ABVD. Проте запропоновано кілька нерандомізованих досліджень, у яких відмічалось, що хворі з поширеною ЛХ із позитивними тимчасовими
результатами ПЕТ мають кращий прогноз після переходу від ABVD до інтенсифікації лікування, ніж після продовження лікування за схемою ABVD [II, B].
Недавнє рандомізоване дослідження продемонструвало підвищення виживання без прогресування хвороби після шести циклів брентуксимабу ведотіну в поєднанні з AVD (A-AVD) порівняно зі стандартною схемою ABVD. Однак A-AVD пов'язують з підвищеною швидкістю виникнення нейропатії і токсичного впливу на кров. Таким чином, необхідні більш тривалі спостереження для отримання остаточних висновків щодо режиму A-AVD [I – II, C]. У
пацієнтів, які отримують BEACOPP у збільшеній дозі, схема лікування може бути безпечно зменшеною до лише чотирьох циклів у разі негативних проміжних результатів ПЕТ, у порівнянні із загальною
кількістю із шести циклів для пацієнтів з позитивними результатами ПЕТ [I, A].
Крім того, застосування променевої терапії може бути
обмеженим у пацієнтів із ПET-позитивними результатами, у яких залишкова лімфома складає 2,5 см після чотирьох циклів, або шести циклів BEACOPP у збільшеній дозі. Кілька досліджень, які випадково порівнювали ABVD і BEACOPP у збільшеній дозі відмітили кращий контроль за пухлинною масою і
тенденцію на шляху до підвищення загальної вижива ності за допомогою BEACOPP у збільшеній дозі. Мета-аналіз, що включав 9993 пацієнтів, також виявив істотне покращення виживання з BEACOPP у збільшеній дозі в порівнянні з ABVD. Виживання збільшилось на 10% за останні 5 років [I, A]. Однак, потрібно враховувати токсичність BEACOPP у збільшеній дозі, під час проведення лікування за даною схемою має бути відповідний нагляд і догляд.
У пацієнтів старше 60 років схема BEACOPP не застосовується, у цій віковій групі спостерігається підвищена смертність, пов'язана з лікуванням [II, A]. Таким чином, ABVD являє собою стандарт лікування ЛХ для пацієнтів літнього віку. У літніх людей, що
приймають більше двох циклів ABVD може виникнути блеоміциніндуковане отруєння, тому пацієнтам старше 60 років потрібно відміняти блеоміцин після другого циклу хіміотерапії [III, B – C].
Рецидив захворювання
Для більшості хворих з рефрактерною або рецидивуючою ЛХ, лікування складається з високодозових схем хіміотерапії (HDCT) з подальшою аутологічною трансплантацією стовбурових клітин
(ASCT) [I, A]. Такі схеми як дексаметазон / високі дози цитарабіну / цисплатин (DHAP), іфосфамід / гемцитабін / винорелбін (IGEV) або іфосфамід / карбоплатин / етопозид (ICE) застосовуються для зниження пухлинного навантаження і мобілізують стовбурові клітини перед HDCT і ASCT [II – III, A]. У деяких пацієнтів одноразове застосування брентуксимабу ведотіну може призвести до негативних результатів ПЕТ і тому його застосування достатньо для “рятівної” терапії перед HDCT і ASCT [III, B].
Використання брентуксимабу ведотіну являє собою варіант лікування пацієнтів, яким не застосовують ASCT. Після основної фази 2-го дослідження, що включало 102 пацієнта з кЛХ з рецидивом після HDCT і ASCT, було продемонстровано загальну частоту відповіді (ORR) 75% при одноразовому застосуванні
брентуксимабу ведотіну. Препарат був схвалений для лікування таких пацієнтів [III, B]. Частка пацієнтів, які досягли довгострокової ремісії, що перевищує 5 років без подальшого лікування, склала 9% [III, B].
Антитіла, спрямовані на запрограмовану смерть клітини 1(PD-1) представляють інший варіант лікування для пацієнтів з множинними рецидивами. Алогенна трансплантація стовбурових клітин представляє
потенційно можливий варіант лікування для пацієнтів, яким неможливо провести HDST і ASC. Такий підхід слід розглядати і обговорювати для молодих хемочутливих пацієнтів із задовільним загальним станом після ретельної оцінки співвідношення факторів
ризику-користі [III, C].
У пацієнтів із множинними рецидивами, які не мають інших варіантів лікування застосовується паліативна хіміотерапія на основі гемцитабіну та / або регіонарної променевої терапії для досягнення прийнятних показників ремісії, підвищення якості життя, збільшення виживання.
Лікування нодулярної форми з переважанням лімфоцитів ЛХ (НФПЛЛХ)
Стадія IA без факторів ризику
Променева терапія залучених ділянок дозою в 30 Гр є стандартом лікуванням стадії IA у пацієнтів НФПЛЛХ без факторів ризику [III, A]. Хоча дані проспективних досліджень доступні тільки про опромінення залучених лімфатичних вузлів, проте поточні рекомендації ILROG рекомендують використовувати опромінення залучених ділянок.
Як правило, НФПЛЛХ лікується ідентично кЛХ у всіх пацієнтів, за винятком пацієнтів зі стадією IA без клінічних факторів ризику [III, B]. Під час ретроспективного дослідження оцінювали комбінацію антиCD20-антитіла і звичайну хіміотерапію виявили перспективні результати з схемою рітуксімаб / циклофосфамід / доксорубіцин / вінкристин / преднізон (R-CHOP)[V, B].
Рецидив НФПЛЛХ
У пацієнтів з підозрою на рецидив НФПЛЛХ до початку терапії необхідно провести біопсію, для виключення трансформації в агресивну неходжкінську лімфому (НХЛ). Згідно з новими даними, швидкість трансформації вище, ніж раніше повідомлялося [IV, A].
Локалізовані форми рецидиву НФПЛЛХ можна ефективно лікувати антитілами проти CD20, такими як ритуксимаб або офатумумаб [III, B].
Пацієнти з більш поширеними формами захворюванням при рецидиві, та з додатковими факторами ризику потребують більш агресивного лікування з хіміотерапією, можливо в поєднанні з
антитілами до CD20 [III, B].
Однак терапію слід підбирати індивідуально і ґрунтуюючись на таких факторах, як час ремісії до початку рецидиву, ступінь захворювання при рецидиві та попереднє лікування [III, B].
Враховуючи відсутність CD30 на злоякісних клітинах, серед яких переважають лімфоцити брентуксимаб ведотін не є варіантом лікування у цьому випадку.
Оцінка відповіді
Якщо не передбачається використання терапії під контролем ПЕТ, проміжну оцінку відповіді можна отримати за допомогою КТ з контрастуванням, яке слід проводити перед променевою терапією в обмеженій та проміжній стадіях і після чотирьох циклів хіміотерапії, а також перед променевою терапією на поширеній стадії. Якщо лікування проводиться під тимчасовим контролем ПЕТ, пацієнти, які отримують ABVD, повинні пройти проміжну ПЕТ-КТ після двох циклів хіміотерапії, незалежно від стадії захворювання.
Пацієнти з поширеною ЛХ, які отримують ABVD, також повинні пройти ПЕТ-КТ після закінчення хіміотерапії. У хворих з поширеною ЛХ, які лікуються за допомогою BEACOPР у збільшеній дозі, ПET-КТсканування повинне проводитися після двох циклів хіміотерапії і
після її закінчення. Остаточна оцінка повинна проводитися після завершення лікування. Фізикальне, лабораторне обстеження та контрастна КТ є обов'язковими.
Прогноз
При сучасних стратегіях лікування у 80%–90% хворих на ЛХ можна досягти постійної ремісії та цих людей можна вважати вилікуваними.
Подальші заходи, відстрочені наслідки та виживаність
Збір анамнезу, фізикальне обстеження та лабораторний аналіз у т.ч. ЗАК, біохімічний аналіз крові проводять кожні 3 місяці протягом першого півріччя, кожні 6 місяців на протягом наступних чотирьох років та надалі один раз на рік [V, B]. КТ і рентгенологічні тести
повинні проводитись один раз для підтвердження статусу ремісії.
Після цього потрібно спостерігати за клінікою пацієнтів.
Сканування
не проводиться, якщо не виявлено клінічних симптомів. Функція щитовидної залози (тиреотропний гормон) повинна оцінюватись один раз на рік, якщо ділянка шиї піддавалася опроміненню. Крім того, слід контролювати рівень тестостерону та естрогену, особливо у молодих пацієнтів з інтенсивною хіміотерапією [V, B].
Пацієнтів слід запитати чи не мають вони скарг, що свідчили б про тривалий токсичний вплив на серце та легені. Скринінг раку повинен проводитися регулярно через постійно підвищений ризик розвитку гематологічних захворювань і виникнення вторинних
злоякісних новоутворень після лікування ЛХ. Особливу увагу слід приділяти скринінгу на рак молочної залози у жінок до 40 років, які отримали опромінення ділянки грудної клітки або пахвової ділянки.
Таким пацієнткам необхідно проводити мамографію раз на рік. Пацієнтам молодше 30 років яким опромінювалась ділянка грудної клітки слід проводити магнітно-резонансну томографію (МРТ) на додаток до мамографії [V, A].