ВІД «ВИДАЛИТИ ВСЕ» ДО ПЕРСОНАЛІЗОВАНОГО БІОЛОГІЧНОГО КОНТРОЛЮ
Ще зовсім недавно міома матки в клінічній логіці описувалася майже лінійно: є доброякісний вузол, який росте під впливом статевих стероїдів, викликає кровотечі, біль, тиск, анемію або репродуктивні проблеми, а отже тактика зводиться до спостереження, тимчасового гормонального контролю або операції.
Ця модель не була хибною. Але сьогодні вже очевидно, що вона була надто спрощеною.
Саме це і є головним підсумком останніх років: у 2024-2026 рр. міома матки перестала виглядати як суто механічна проблема вузла і дедалі більше розглядається як біологічно складний процес, у якому переплітаються соматичні мутації, клітинна гетерогенність, фібротичне ремоделювання тканини, гормональна регуляція, системні коморбідні зв’язки та різні клінічні сценарії.
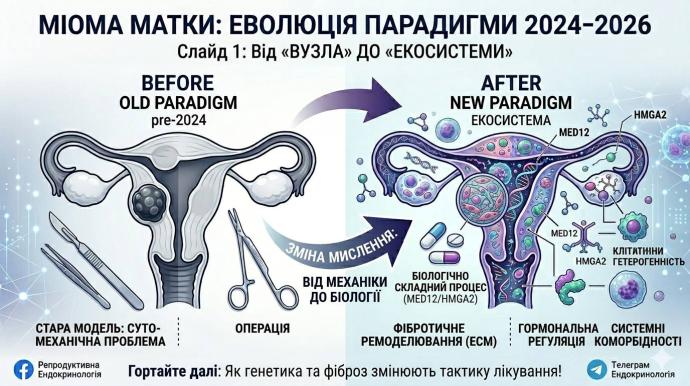
Що саме змінилося в патогенезі?
Сучасні огляди не заперечують гормональну залежність міоми. Естроген і особливо прогестерон залишаються фундаментальними для росту пухлини. Але тепер ми бачимо значно повнішу картину.
Міома виникає не просто як наслідок “надлишку гормонів”, а як результат соматичної мутації у клітині-попереднику міометрію, після чого вже диференційовані клітини пухлини і пухлино-асоційовані фібробласти формують надлишковий extracellular matrix (позаклітинний матрикс, ECM — мережа колагену та інших структурних білків, що визначає жорсткість і механіку тканини).
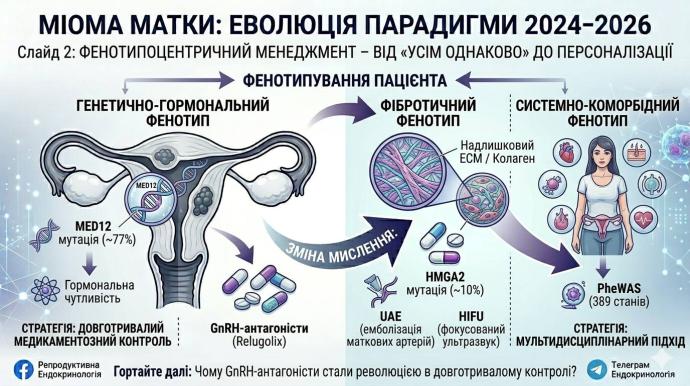
У великому огляді Physiological Reviews підкреслено, що найчастіші драйверні мутації стосуються MED12 (ген mediator complex subunit 12 — ключовий регулятор транскрипції, що впливає на проліферацію клітин міометрію) — приблизно 77%, а HMGA2 (ген high mobility group AT-hook 2 — регулятор росту та клітинної проліферації) — близько 10%. Надмірне відкладення ECM є настільки характерною рисою, що саме воно історично закріпило за цими пухлинами назву fibroids.
Тобто нова парадигма не скасовує гормональну модель, а вбудовує її у ширший генетично-клітинний і фіброз-орієнтований контекст.
Клінічно це важливо ще й тому, що такі генетичні драйвери частково пояснюють, чому одна пацієнтка демонструє виражену гормональну чутливість і ріст вузлів, тоді як інша — значно слабшу або неоднорідну відповідь на ті самі гормональні стимули.
Було: “однорідний вузол”. Стало: “гетерогенна екосистема”
Одне з найбільш концептуальних зрушень принесла single-cell RNA sequencing (одноклітинне секвенування РНК, scRNA-seq — метод, що дозволяє аналізувати експресію генів на рівні окремих клітин).
Огляд AJOG, присвячений аналізу міом на рівні single-cell RNA sequencing, показав, що вузол не є однорідною клітинною масою. Дослідники описують щонайменше три різні популяції гладеньком’язових клітин (міоцитів) та окремі популяції фібробластів.
Ще важливіше те, що не всі міоцити в MED12-мутантних міомах самі несуть мутацію MED12.
Чому це критично? Тому що якщо раніше вузол розуміли як однорідний об’єкт, який більш-менш однаково реагує на терапію, то тепер дедалі очевидніше, що перед нами клітинно гетерогенна тканинна екосистема.
Це пояснює: різну відповідь на гормональну терапіюваріабельність росту вузлівпотенційні механізми резистентності
Чи є міома лише локальною патологією матки?
Ще одна важлива зміна стосується системного погляду на хворобу.У 2025 році в Communications Medicine було опубліковано phenome-wide association study (PheWAS — аналіз асоціацій по всьому феному) — підхід, що дозволяє оцінити зв’язки одного захворювання з широким спектром інших станів.
У мультипопуляційному метааналізі автори виявили 389 станів, асоційованих із фібромами, з enrichment для циркуляторних, дерматологічних, урогенітальних, м’язово-скелетних та сенсорних захворювань.
Серед найбільш клінічно цікавих асоціацій — артеріальна гіпертензія, порушення ліпідного обміну, ожиріння та інші метаболічні зрушення, тобто саме ті стани, які лікарі часто сприймають як “паралельний фон”, а не як частину ширшого біологічного контексту хвороби.
Це не означає, що міома вже доведено є системною хворобою в жорсткому причинно-наслідковому сенсі. Але це точно означає, що сучасна наука більше не підтримує вузьке уявлення про неї як про суто локальну проблему матки.
Академічно точніше сказати так: міома має виражений системний коморбідний контекст.
Як було і як стало: справжня зміна парадигми
- Було: міома = доброякісний гормонозалежний вузол, який або спостерігають, або тимчасово пригнічують, або видаляють.
- Стало: міома = доброякісна гормонозалежна пухлина з вираженим фібротичним фенотипом, генетичними драйверами, клітинною гетерогенністю та системним коморбідним контекстом.
- Було: ключове мислення — органоцентричне й вузлоцентричне.
- Стало: ключове мислення — фенотипоцентричне і персоналізоване.
- Було: основна вісь рішень — “коли оперувати”.
- Стало: основна вісь рішень — “яка біологія захворювання, які симптоми, які репродуктивні плани, чи можливий тривалий контроль без радикального втручання”.
Сучасна терапія: головний практичний зламНайважливіша зміна останніх років полягає в тому, що медикаментозна терапія перестає бути лише коротким “містком до операції” і стає самостійною стратегією довготривалого контролю симптомів у частини пацієнток.
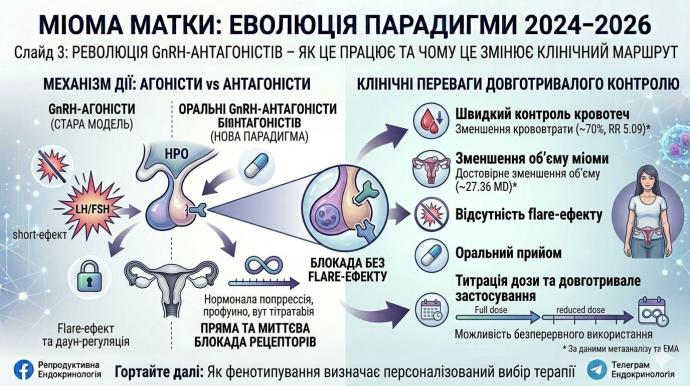
Що було раніше?Стара модель ґрунтувалася переважно на GnRH (гонадотропін-рилізинг гормон) агоністах, які застосовувалися передопераційно. Вони могли зменшувати об’єм вузлів і крововтрату, але їх тривале застосування обмежувалося:flare-ефектом,гіпоестрогенними проявами,ризиком втрати кісткової маси,поганою придатністю для довготривалого контролю.
FIGO best practice guidance 2025 прямо нагадує, що GnRH analogs переважно мають передопераційне значення саме через несприятливий профіль довготривалих небажаних ефектів.
Що стало тепер? Головний сучасний поворот пов’язаний із оральними GnRH (гонадотропін-рилізинг гормон) антагоністами.Метааналіз 2025 року в Archives of Gynecology and Obstetrics, який включив 11 рандомізованих клінічних досліджень і 4164 пацієнток, показав, що GnRH-антагоністи забезпечують статистично значуще покращення контролю маткової кровотечі порівняно з плацебо: RR (відносний ризик) 5,09; 95% ДІ (довірчий інтервал) 3,19-8,14.Крім того, вони зменшують об’єм фібром: MD −27,36; 95% ДІ від −38,89 до −15,83.
Це вже не теоретична перспектива, а доказовий масив, який реально змінює клінічну практику.
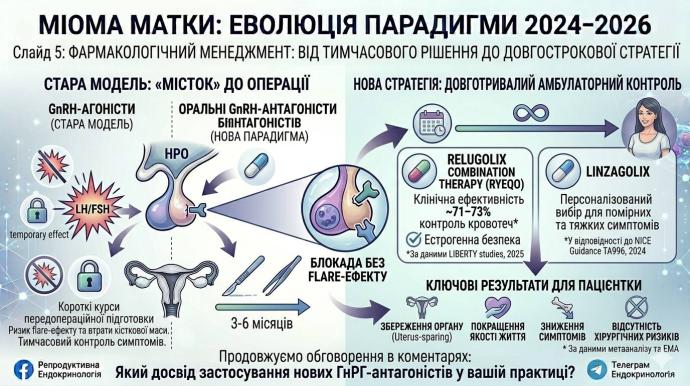
Relugolix combination therapy: символ сучасної ериНайбільш показовим прикладом є relugolix combination therapy — комбінована терапія: антагоніст GnRH релуголікс + естрадіол + норетистерону ацетат. Така комбінація дозволяє одночасно контролювати симптоми міоми та знижувати ризик гіпоестрогенних побічних ефектів.
За даними EMA, у двох дослідженнях за участю жінок репродуктивного віку з heavy menstrual bleeding, приблизно по 500 пацієнток у кожному, Ryeqo продемонстрував переконливу клінічну ефективність.
У першому дослідженні:
73% жінок, які отримували relugolix combination therapy, досягли значущого зменшення крововтратипроти 19% у групі плацебо
У другому:
71%проти 15% відповідноEMA також зазначає, що препарат може застосовуватися без перерви.
Саме це і є справжньою зміною мислення:ми переходимо від коротких курсів тимчасового пригнічення до можливості тривалішого амбулаторного контролю симптомів.
Linzagolix: не просто ще один препарат
У серпні 2024 року NICE випустив guidance TA996, де надав evidence-based recommendations щодо linzagolix (пероральний селективний GnRH-антагоніст із можливістю гнучкого дозування) для лікування помірних і тяжких симптомів фібром у дорослих репродуктивного віку. Цінність цього препарату не лише в тому, що він поповнює список доступних опцій. Його значення в іншому: він уособлює сучасний відхід від жорсткої уніфікації лікування.
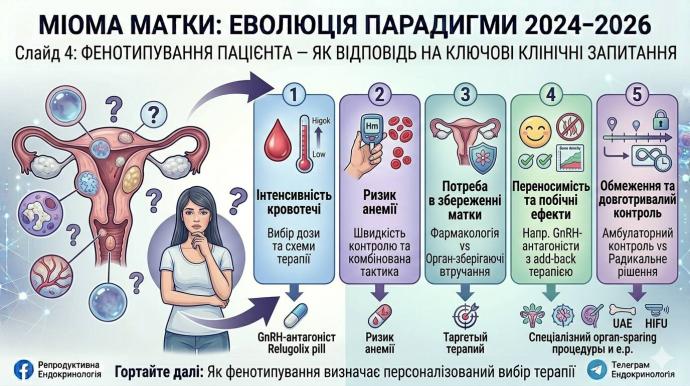
Сьогодні ми говоримо вже не просто про “гормональну терапію”, а про індивідуалізоване фармакологічне керування симптомами з урахуванням: інтенсивності кровотечі, ризику анемії, потреби в збереженні матки,переносимості,обмежень довготривалого лікування.
Для практичної української аудиторії важливо й інше: ці підходи більше не сприймаються як суто “теоретичні західні опції”. Нові препарати та комбіновані схеми поступово входять у поле реального клінічного обговорення через офіційний імпорт, приватний сектор і зростання інтересу до organ-sparing менеджменту, хоча питання доступності, вартості та широкої аптечної присутності все ще залишаються суттєвим обмеженням.
А хірургія зникла? Ні. Але змінилося її місце
Було б помилкою створити враження, що нова парадигма “скасовує” операцію.
Насправді хірургія не зникає. Змінюється її місце в алгоритмі.
Сучасна гінекологія відходить не від операцій як таких, а від автоматизму, за яким гістеректомія сприймалася як майже неминуче остаточне рішення. Сьогодні значно активніше розвиваються organ-sparing та image-guided підходи:
UAE (uterine artery embolization — емболізація маткових артерій) — метод, що зменшує кровопостачання вузлів і спричиняє їх ішемічну редукцію
RFA (radiofrequency ablation — радіочастотна абляція) — локальне термічне руйнування тканини міоми
HIFU (high-intensity focused ultrasound — високоінтенсивний фокусований ультразвук) — неінвазивна абляція тканини за допомогою сфокусованого ультразвуку
Огляд IJGO 2025 року прямо наголошує, що ці техніки особливо корисні для жінок, які хочуть зберегти матку, мають протипоказання до операції або бажають уникнути більш інвазивного втручання.
Отже, мета формулюється вже не як “позбутися вузла будь-якою ціною”, а як“контролювати симптоми, мінімізувати шкоду, зберегти орган і врахувати репродуктивні плани там, де це можливо”.
Актуальність для України
Для українського контексту ця зміна парадигми має особливе значення.
Наші клінічні маршрути досі часто тяжіють до сценарію, де симптомна міома швидко переходить у площину оперативного рішення, особливо якщо пацієнтка має анемію, множинні вузли або тривалий анамнез кровотеч.
Але нова міжнародна література змушує ставити питання інакше.
Не “чи потрібна операція взагалі?”, а: яка біологія захворювання у цієї пацієнткиякий у неї фенотип симптомівякі репродуктивні планичи можна стабілізувати стан медикаментозночи є підстави для organ-sparing інтервенційного підходуі де саме операція справді дає найкраще співвідношення користі та ризику
Тобто сучасне мислення — це не спрощення, а навпаки, ускладнення клінічного рішення заради кращої персоналізації.
Висновки
Станом на 2024–2026 роки міома матки вже не вкладається у стару схему “гормони → вузол → операція”.
Сучасні дані показують, що це: гормонозалежна доброякісна пухлиназ вираженим фібротичним фенотипомгенетичними драйверамиклітинною гетерогенністюі системним коморбідним контекстом
А головний терапевтичний висновок такий: епоха оральних GnRH-антагоністів змінила не лише список препаратів, а саму логіку лікування міоми.Сучасна терапія — це вже не тільки про зменшення вузла.Це про довготривале, контрольоване і персоналізоване управління хворобою.
Критичний погляд редакції
Попри переконливість сучасної парадигми, важливо уникати її некритичного перенесення у щоденну практику.По-перше, більшість даних щодо GnRH-антагоністів базується на рандомізованих клінічних дослідженнях із відносно обмеженою тривалістю спостереження. Питання довгострокової безпеки (кісткова тканина, серцево-судинні ризики, метаболічні ефекти) потребують подальшого накопичення real-world evidence.
По-друге, фенотипоцентричний підхід виглядає концептуально привабливо, але в реальній клініці він часто стикається з обмеженнями: відсутність доступу до молекулярного профілюванняваріабельність інтерпретації фенотипівзалежність від досвіду лікаря та ресурсів закладу
По-третє, асоціації, виявлені в PheWAS-дослідженнях, не означають причинно-наслідкових зв’язків. Існує ризик надмірної інтерпретації коморбідностей як частини єдиного патогенетичного процесу.
Окремо варто враховувати український контекст: доступність сучасних препаратів (relugolix, linzagolix), їх вартість, а також відсутність чітко адаптованих національних рекомендацій можуть обмежувати впровадження нової парадигми.
Таким чином, сучасний підхід до міоми матки — це не заміна “старого на нове”, а розширення клінічного інструментарію, яке вимагає зваженого, індивідуалізованого та ресурсно-орієнтованого застосування.
Що це змінює вже завтра в кабінеті лікаря
Сучасна парадигма міоми матки — це не про “нові препарати”, а про зміну логіки прийняття рішень.
Замість автоматичного переходу до операції:
— оцінити, чи можна стабілізувати стан медикаментозно
Замість орієнтації лише на розмір вузла:
— оцінити фенотип пацієнтки (кровотеча, анемія, симптоми, репродуктивні плани)
Замість короткострокових рішень:
— розглядати довготривалий контроль симптомів як реальну стратегію
Замість “одного правильного методу”:
— комбінувати підходи (фармакотерапія + інтервенційні методи)
І головне:
— пояснювати пацієнтці, що міома — це не вирок до операції, а керований стан
Тобто ключове питання змінюється:
не “як швидше позбутися вузла?”
а “як найкраще контролювати захворювання саме у цієї пацієнтки?”
Питання до обговорення
Чи готові ми в українській практиці перейти від вузлоцентричного мислення до фенотипоцентричного менеджменту міоми?
І чи не настав час розглядати сучасну медикаментозну терапію не як тимчасовий компроміс, а як повноцінний компонент довгострокової стратегії лікування?